Определение глюкозы в крови
Методы объемного анализа, приготовление титрованных растворов, индикаторов, подготовка посуды изложены в предшествующих курсах техники лабораторных работ, аналитической химии, общей биохимии и пр. В данном руководстве приведены лишь биохимические методы исследования, предусмотренные программой.
В лабораториях пользуются для колориметрирования спектрофотометром или фотоэлоктроколориметром. Если этих приборов нет, то используют колориметр Дюбоска или Аутенрита.
Для проведение данных исследований необходимо следующее оснащение рабочего места:
- Штативы.
- Капельницы.
- Градуированные пипетки на 1, 2, ,5 и 10 мл.
- Пипетка Мора на 2 мл.
- Химические пробирки.
- «Сахарные» пробирки (высота 16 см, диаметр 2-2,5 см).
- «Сахарные» воронки.
- Колбочки на 50 мл.
- Колбочки на 100 мл.
- Прокипяченная и высушенная вата.
- Водяная баня.
- Песочные часы на 15 минут.
- Микропипетки на 0,1 мл.
- Набор для взятия крови.
- Сернокислый цинк (ZnS04).
- Едкий натр (NaOH).
- Красная кровяная соль (железосинеродистый калий) — K3[Fe(CN)6].
- Хлористый натрий (NaCl).
- Йодистый калий (KJ).
- Ледяная уксусная кислота.
- Гипосульфит натрия (Na2S203 • 5Н20).
- Растворимый крахмал.
- Йодноватистокислый калий (KJO3).
Определение глюкозы в крови по способу Хагедорна-Иенсена
Принцип метода основан на способности глюкозы вступать в окислительно-восстановительные реакции. Глюкоза, окисляясь, восстанавливает в щелочной среде железо красной кровяной крови, превращая ее в желтую. Невосстановленную красную кровяную соль определяют йодометрически: по количеству восстановленной красной кровяной соли определяют количество глюкозы в крови.

Для этого метода используют следующие реактивы:
- 45% раствор сернокислого цинка: 45 г химически чистого сернокислого цинка помещают в колбочку на 100 мл и доливают дистиллированной водой до метки 100 мл. Реактив стоек.
- 0,45% раствор сернокислого цинка. Реактив готовят из 45% раствора сернокислого цинка: 1 мл 45% раствора сернокислого цинка помещают в колбочку емкостью 100 мл и доливают дистиллированной водой до метки 100 мл; реактив готовят каждую неделю.
- 0,1 N раствор NaOH. Поскольку в едком натре содержатся углекислые соли и вода, приготовить точный раствор его при растворении навески вещества невозможно. Поэтому вначале готовят насыщенный водный раствор химически чистой едкой щелочи.
Насыщенный раствор едкого натра ввиду сильного его разогревания приготовляют в толстостенной посуде. Хранить реактив рекомендуется в бутылке, внутренние стенки которой покрыты парафином, иначе стекло посуды постепенно выщелачивается. Приготовленный насыщенный раствор NaOH отстаивается в течение 2-3 дней. Затем в мерную колбочку на 250 мл наливают 1,75 мл насыщенного раствора NaOH и доливают до метки свежепрокипяченной и остуженной дистиллированной водой.
Титр приготовленного раствора едкого натра устанавливают путем титрования его точным раствором 0,1 N щавелевой кислоты следующим образом. В три колбочки отмеривают по 20 мл 0,1 N раствора щавелевой кислоты и прибавляют по 1-2 капли 1% спиртового раствора фенолфталеина.
В бюретку наливают приготовленный раствор едкого натра и титруют им 0,1 N раствор щавелевой кислоты в каждой колбочке до появления красного окрашивания. Учитывают количество едкого натра, пошедшего на титрование содержимого каждой колбочки, выводят средне-арифметическое и рассчитывают коэффициент поправки.
Затем количество миллилитров приготовленной щелочи умножают на коэффициент поправки и доливают дистиллированной водой до объема, полученного в результате расчета.
Пример расчета: объем исходного раствора щелочи 450 мл, коэффициент поправки 1,024: 450X1,024=460,8 мл.
Доводим исходный объем щелочи дистиллированной водой до 460,8 мл. Титр разведенного таким образом раствора еще раз проверяют титрованием точного раствора 0,1 N щавелевой кислоты.
4. 0,005 N раствор красной кровяной соли. Реактив готовят из перекристаллизованной красной кровяной соли. Перекристаллизацию проводят следующим образом. Кристаллы красной кровяной соли помещают в фарфоровую чашку, промывают несколькими порциями холодной воды и растворяют в небольшом количестве кипящей дистиллированной воды. Раствор фильтруют в горячем виде через предварительно промытый горячей дистиллированной водой фильтр в фарфоровую чашку (чашку помещают на лед или холодную воду). Образовавшиеся кристаллы сушат в сушильном шкафу или термостате при температуре 50°. Высушенные кристаллы хранят в тщательно закрытой банке в темном месте. Процесс перекристаллизации проводят при искусственном освещении.
Для приготовления реактива на аналитических весах взвешивают 1,65 г перекристаллизованной красной кровяной соли и навеску количественно переносят в мерную колбу емкостью 1 л. На технических весах взвешивают 10,6 г безводной соды. Для обезвоживания перед взвешиванием соду прокаливают и охлаждают в эксикаторе. Навеску безводной соды помещают в ту же мерную колбу. Вначале ее растворяют в небольшом количестве воды, а затем приливают дистиллированную воду до метки. Приготовленный раствор хранят в посуде из темного стекла в прохладном месте.
5. Тройной реактив (хлор-цинк-йодистый реактив): 50 г химически чистого сернокислого цинка и 250 г хлористого натрия растворяют в 1 л воды и фильтруют; реактив стоек. Перед употреблением реактива в нем растворяют 2,5 г йодистого калия.
6. 3% раствор уксусной кислоты: 3 мл ледяной уксусной кислоты помещают в колбу на 100 мл и доводят дистиллированной водой до метки.
7. 0,005 N раствор гипосульфита натрия. Реактив готовят из 0,1 N раствора в момент постановки опыта. На технических весах взвешивают 25 г химически чистого гипосульфита натрия, растворяют в 1 л свежепрокипяченной и остывшей дистиллированной воды и оставляют на 8-14 дней в хорошо закупоренной посуде из темного стекла. Для приготовления 0,005 N раствора отмеривают 5 мл 0,1 N раствора гипосульфита в мерную колбу емкостью 100 мл и доливают дистиллированной водой до метки.
8. 0,005 N раствор йодноватистокислого калия. Вначале готовят 0,1 N раствор йодноватистокислого калия, для чего на аналитических весах взвешивают 7,134 г KJO3, эту навеску растворяют в дистиллированной воде и доводят ее объем в мерной колбе на 1 л до метки. Раствор стоек.
Для прпготовлеппя 0,005 N раствора KJO3 5 мл 0,1 N раствора йодноватистокислого калия наливают в мерную колбу на 100 мл и доводят дистиллированной водой до метки.
9. 1 % раствор крахмала: в колбочку на 100 мл наливают 50 мл насыщенного (35%) раствора поваренной соли и кипятят его. 1 г растворимого крахмала взбалтывают в пробирке в нескольких миллилитрах дистиллированной воды и выливают при помешивании в кипящий насыщенный раствор поваренной соли; кипятят до просветления раствора, охлаждают и доводят до 100 мл насыщенным раствором хлористого натрия. Раствор сохраняет стойкость на неограниченный срок; с йодом дает синее окрашивание.
Техника определения глюкозы в крови
1. Для определения глюкозы в крови подготавливают четыре химические пробирки, нумеруют их и устанавливают в штатив. Первые две пробирки предназначаются для опытных проб, а две другие — для контролей.
2. Во все четыре пробирки наливают по 5 мл 0,45% раствора сернокислого цинка, по 1 мл 0,1 N раствора едкого натра и смешивают; получают хлопьевидную взвесь гидрата окиси цинка.
3. В первые две пробирки микропипеткой вносят по 0,1 мл крови, взятой у больного из пальца натощак. Затем кончик микропипетки тщательно вытирают, проверяют точность взятия крови и погружают микропипетку в жидкость. Кровь выдувают на дно пробирки, а микропипетку тщательно прополаскивают бесцветным раствором из верхнего слоя жидкости, после чего содержимое пробирок смешивают.
4. Все четыре пробирки ставят в кипящую водяную баню на 3 минуты. При кипячении в первых двух пробирках белки крови свертываются и образуют серовато-коричневый сгусток. В контрольных пробирках сгусток не образуется.
5. После трехминутного кипячения пробирки вынимают из водяной бани и охлаждают.
6. После охлаждения содержимое каждой пробирки встряхивают. При этом в первых двух пробирках разбиваются образовавшиеся сгустки.
7. В специальный штатив устанавливают четыре «сахарные» пробирки и нумеруют соответственно опытным и контрольным химическим пробиркам. В «сахарные» пробирки вставляют «сахарные» воронки с фильтром из прокипяченной и высушенной ваты. Ватный фильтр смачивают дистиллированной водой.
Содержимое каждой химической пробирки выливают на ватный фильтр соответствующей «сахарной» воронки. Пробирки дважды споласкивают каждый раз 3 мл дистиллированной воды и воду выливают в те же воронки. Капли воды, оставшиеся в узкой части воронки, стряхивают в пробирку или отжимают, надавливая ладонью на воронку. Получают прозрачный бесцветный фильтрат.
8. Во все «сахарные» пробирки приливают точно по 2 мл 0,005 N раствора красной кровяной соли.
9. Пробирки ставят в кипящую водяную баню на 15 минут.
10. За это время готовят хлор-цинк-йодистый реактив (тройной) и определяют титр 0,005 N раствора гипосульфита натрия по 0,005 N раствору KJO3. С этой целью в колбочку наливают точно 2 мл 0,005 N раствора йодноватистокислого калия, 3 мл тройного реактива, 2 мл уксусной кислоты, 2-3 капли 1% раствора крахмала и титруют 0,005 N раствором гипосульфита натрия из микробюретки до обесцвечивания раствора. Отмечают цифру ушедшего на титрование гипосульфита.
Пример расчета. На титрование 2 мл 0,005 N раствора йодноватистокислого калия ушло 1,94 мл гипольсуфита. Поправочный коэффициент гипосульфита: 2: 1,94 = 1,03.
Поправочный коэффициент учитывают при вычислении результатов определения, т. е. результат каждого определения умножают на 1,03. Поправочный коэффициент гипосульфита натрия можно определить по точно приготовленному 0,005 N раствору K3[Fe(CN)6]. Данные проверки по обоим исходным веществам — KJO3 и K3[Fe(CN)6l — должны быть одинаковыми. Поправочный коэффициент гипосульфита натрия определяют каждый раз перед титрованием проб.
11. По истечении 15 минут с водяной бани снимают «сахарные» пробирки и охлаждают их.
12. Во все пробирки приливают по 3 мл тройного реактива и по 2 мл 3% уксусной кислоты.
13. Непосредственно перед титрованием в каждую пробирку наливают по 2-3 капли 1% раствора крахмала. Так как в растворе содержится свободный йод, то с крахмалом он дает синее окрашивание.
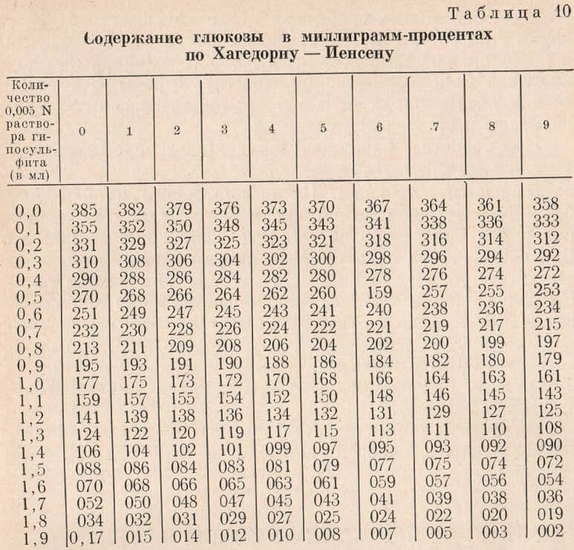
14. Каждую из полученных проб титруют 0,005 N раствором гипосульфита натрия. Начинают титрование с контролей, а затем переходят к титрованию опытных проб. Титрование проводят следующим образом. К каждой пробе приливают по каплям из бюретки 0,005 N раствор гипосульфита натрия до момента полного обесцвечивания. Отмечают количество гипосульфита натрия, пошедшего на титрование. При правильно проведенном титровании разница между объемами гипосульфита натрия, пошедшего на титрование параллельных проб, не должна превышать 0,01 — 0,02 мл. Расчет содержания глюкозы в крови производят по табл. 10.
Пример расчета. Предположим, что на титрование содержимого контрольных пробирок (Ki и Кг) соответственно израсходовано 1,96 и 1,98 мл 0,005 N раствора гипосульфита натрия и на титрование опытных пробирок (Oi и 02) — 1,4 и 1,42 мл 0,005 N раствора гипосульфита натрия. Вычисляют среднее арифметическое из полученных данных.
Таким образом, на титрование содержимого каждой контрольной пробирки израсходовано 1,97 мл, а на титрование опытных пробирок — 1,41 мл 0,005 N раствора гипосульфита натрия.
Затем по таблице определяют количество глюкозы в миллиграмм-процентах следующим образом. В крайнем вертикальном столбце таблицы отыскивают целые и десятые миллилитра 0,005 N раствора гипосульфита натрия, ушедших на титрование, в верхнем горизонтальном столбце находят сотые. На пересечении соответствующих цифр таблицы находят цифру глюкозы, выраженную в миллиграммах на 100 мл крови (мг%). Таким образом, цифре 1,97 соответствует 5 мг%, а цифре 1,41 — 104 мг% глюкозы. Окончательную цифру получают путем вычитания результатов, полученных в контрольных пробах (так как реактивы обладают способностью восстанавливать красную кровяную соль), из результатов, полученных в опытных пробах 104—5 = 99 мг%.
Если в опытных пробирках после 15-минутного кипячения происходит обесцвечивание раствора, необходимо в пробирки добавить еще 2 мл 0,005 N раствора красной кровяной соли и снова прокипятить пробы в течение 15 минут. Пробирки охладить, прибавить все остальные реактивы и протитровать.
При расчете к найденной по таблице цифре глюкозы в миллиграмм-процентах прибавляют 385.
Пример расчета. После повторного прибавления 0,005 N раствора красной кровяной соли на титрование контролей израсходовано соответственно 1,96 и 1,98 мл 0,005 N раствора гипосульфита натрия, а на титрование опытных пробирок — 1,5 и 1,52 мл 0,005 N раствора гипосульфита натрия. Среднее арифметическое для контролей равно 1,97 мл, что соответствует 5 мг% глюкозы: среднее арифметическое для опытных проб равно 1,51, что соответствует 86 мг% глюкозы.
Ответ. Содержание глюкозы в крови равно: 385 + + 86-5 = 466 мг%.
Результаты определений оформляют в бланке анализа. В крови здоровых людей содержится от 70 до 120 мг% глюкозы.