Исследование и определение глюцидов в моче
В норме моча содержит весьма незначительные количества глюкозы (350–500 мг/сутки), которые не могут быть выявлены методами, обычно применяемыми при анализе глюкозы в моче. В основе этих методов лежит восстановительная способность глюкозы и так как моча содержит кроме того и другие восстановительные вещества (мочевую кислоту, ураты, креатинин и др.) их необходимо предварительно удалить с помощью подходящего вещества таким образом, чтобы фильтрат содержал только глюкозу.
Осаждение реактивом Куртона
Реактивы. 300 г ацетата натрия растворяют в 900 мл дистиллированной воды, нейтрализуют ледяной уксусной кислотой (индикатор лакмусовая бумажка), фильтруют в мерную колбу на 1 000 мл и дополняют дистиллированной водой до метки.
Техника. К 9 мл мочи добавляют 1 мл реактива Куртона, энергично встряхивают и фильтруют. Если фильтрат не прозрачный, первые порции фильтруют повторно на том же фильтре. Этот способ применяется в лаборатории наиболее часто, являясь менее сложным и давая удовлетворительные результаты.
Осаждение реактивом Патейна
Реактивы. 200 г нитрата ртути растворяют в 600 мл дистиллированной воды, подщелачивают (индикатор – лакмусовая бумажка) раствором едкого натра 10%. Переводят в мерную колбу на 1 000 мл и дополняют дистиллированной водой до метки. Или: 200 г красной окиси ртути растворяют в 160 мл концентрированной азотной кислоты (уд. вес. = 1,40) в фарфоровой чашке. Хорошо смешивают стеклянной палочкой во избежание комков, которые в случае необходимости разбиваются пестиком. Через 5 минут добавляют 160 мл дистиллированной воды и нагревают до кипения. После полного растворения окиси ртути, охлаждают, затем добавляют 30 мл едкого натра 10%, перемешивая стеклянной палочкой. Переводят в мерную колбу на 1 000 мл, дополняют дистиллированной водой до метки и затем фильтруют. Реактив не подвергается порче.
Техника. В ступку берут 50 мл мочи и 25 мл реактива Патейна, смешивают пестиком и нейтрализуют едким натром 10% по отношению к лакмусу. Затем переводят в мерный цилиндр на 100 мл, споласкивая дистиллированной водой и дополняя до 100 мл. Фильтруют. Фильтрат должен быть бесцветным и нейтральным. Для удаления ртути, фильтрат обрабатывают 1 г цинкового порошка и встряхивают. Фильтруют снова, затем фильтрат доводится до щелочной реакции к лакмусу едким натром 10%.
Приечание. Моча больных, леченных инсулином, обязательно осаждается реактивом Патейна, ибо в противном случае реакция восстановления раствора Фелинга не бывает четкой.
Качественный анализ глюкозы
Метод Фелинга
Принцип. Реакция основывается на свойстве глюкозы, в связи с ее альдегидной функцией, восстанавливать при нагревании в щелочной среде гидрат меди синего цвета в недоокись меди кирпично-красного цвета.
Реактив Фелинга состоит из двух растворов:
Фелинг : в мерной колбе на 1 000 мл растворяют 35 г сульфата меди в дистиллированной воде, добавляют 5 мл концентрированной серной кислоты и дополняют дистиллированной водой до метки.
Фелинг II : Смешивают 150 г сегнетовой соли (двойной тартрат натрия и калия, кристаллический, чистый) с 300 мл раствора едкого натра 30% (чистого, некарбонатированного) в мерной колбе на 1000 мл и дополняют дистиллированной водой до метки.
Техника. В пробирку из иенского стекла берут 2 мл смешанного реактива Фелинга и нагревают до кипения. Реактив не должен изменять своего цвета. Затем добавляют 2 мл подвергнутой осаждению мочи реактивом Куртона и снова нагревают до кипения верхнюю часть жидкости, держа пробирку в наклонном положении. Если моча содержит глюкозу, то получается кирпично-красный осадок. Цвет и количество осадка зависят от концентрации глюкозы в исследуемом образце.
Примечание. Неочищенная моча, содержащая менее 4 г/л глюкозы, дает отрицательную реакцию Фелинга, в то время как при очищенной моче реакция Фелинга бывает отрицательной только, если моча содержит менее 3 г/л глюкозы. Водный раствор чистой глюкозы повышает чувствительность реакции до 0,50 г/л глюкозы.
Метод Бенедикта
Принцип тот же, что и при применении реакции Фелинга.
Реактив Бенедикта: растворяют 173 г цитрата натрия в 600 мл горячей дистиллированной воды, затем добавляют 100 г безводного карбоната натрия или 180 г кристаллического карбоната натрия. Встряхивают до полного растворения, затем фильтруют в мерный цилиндр на 1 000 мл, в который добавляют помешивая стеклянной палочкой 17,3 г сульфата меди, растворенного в 100 мл горячей воды. После охлаждения объем дополняют до 1 000 мл дистиллированной водой.
Техника. В пробирку из иенского стекла берут 5 мл реактива Бенедикта и добавляют 5 капель очищенной мочи. Пробирку погружают в кипящую водяную баню на 5 минут. В норме цвет мочи остается без изменения. Если моча содержит глюкозу, то появляется характерный типичный красный осадок недоокиси меди.
Этот метод более чувствителен, чем метод Фелинга.
Метод Ниландера
Принцип этого метода также основывается на свойстве альдегидной функции глюкозы восстанавливать соли тяжелых металлов; в данном случае азотат висмута восстанавливается до металлического висмута, имеющего черный цвет.
Реактив Ниландера: растворяют 100 г нитрата натрия, 40 г сегнетовой соли и 20 г нитрата висмута в дистиллированной воде, затем объем дополняют до 1000 мл.
Техника. К 10 мл очищенной мочи добавляют 1 мл реактива Ниландера, затем погружают на 7 минут в кипящую водяную баню. В присутствии глюкозы происходит восстановление нитрата висмута в черный металлическии висмут.
Примечание. Реакция весьма чувствительна, но все же, если результат положительный, ее необходимо проверить реакцией Феллинга или Бенедикта, имея в виду возможность того, что черный осадок был образован не металлическим висмутом, а сульфидом висмута, образовавшимся из ряда серосодержащих веществ (цистин, альбумин и др.), которые могут быть выделены мочой.
Тест с фенилгидразином
Принцип. Моно- и двусахариды соединяются с фенилгидразином посредством альдегидной или кетоновой группы и дают продукты конденсации, вызываемые озазонами (в случае глюкозы получается глюкоозазон). Реакция происходит в трех фазах: одна молекула оза присоединяется к молекуле фенилгидразина и дает фенилгидразон (1), который с еще одной молекулой фенилгидразина дает промежуточный продукт (II), а этот последний с другой молекулой фенилгидразина дает озазон (III).
Техника. В пробирку берут 0,5 мл жидкого фенилгидразина, 1 мл ледяной уксусной кислоты и 1 мл ацетата натрия 25%, затем добавляют около 10 мл мочи, очищенной реактивом Патейна, которым удаляют все остальные восстановительные вещества, которые может содержать моча, переводя в фильтрат только глюциды. Фильтруют, после чего пробирку выдерживают в течение 1 часа в кипящей водяной бане, а затем немедленно фильтруют в горячем состоянии в другую пробирку, которую охлаждают вместе с водяной баней. В присутствии глюкозы получается озазон, нерастворимый в горячем состоянии, который остается во втором фильтре, в котором при исследовании под микроскопом наблюдается присутствие расположенных в виде пучков желто-золотистых игл (рис. 44) с точкой плавления= 200–205°. Если моча содержит также лактозу или мальтозу, их озазоны кристализуют в последней пробирке на холоду.
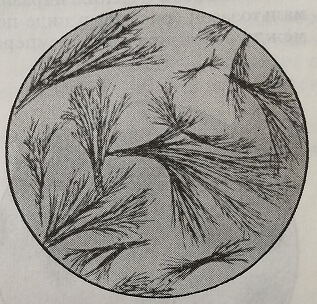
Рис. 44. Кристаллы глюкозазона.
Примечание. Эту реакцию применяют для выявления или качественного анализа глюцидов в количестве менее 3–4 г/л, которые, как мы видели раньше, не могут быть определены другими методами. Чувствительность реакции к фенил- гидразину доходит до 10 мг глюкозы.
Если в горячем состоянии осадок не появляется – что обычно случается, когда количество глюкозы не превышает 1 г/л, содержание пробирки переводят в центрифужную пробирку с коническим дном и отставляют в покое в прохладном месте на 9–12 часов, затем центрифугируют, а собранный пипеткой Пастера осадок рассматривают под микроскопом с окуляром 2 и объективом 7 или с иммерсией. В этом случае иглы глюкозазона кажутся расположенными в виде «игл ежа». .Макроскопический осадок можно различить после центрифугирования до 0,10 г глюкозы/л.
Исследование других восстановительных глюцидов
Кроме глюкозы, моча может содержать также и другие глюциды, обладающие восстановительными свойствами: лактозу, мальтозу, левулозу, полисахариды и пентозы. Восстановительные свойства имеют также декстрины, альбумин, (оксимаслянная кислота и глюкуроновые соединения (продукты сопряжения с фенолом), которые можно, однако, удалить осаждением реактивом Патейна, за исключением (3-оксимасляной кислоты, переходящей в фильтрат.
Лактоза дает с фенилгидразином в холодном состоянии, характерный лактозазон (рис. 45) в виде лучеобразных сфероидов с температурой кипения = 213–215°.

Рис. 45. Кристаллы лактозазона.
Тест Рубнера служит для дифференцирования глюкозы от лактозы. К 10 мл мочи добавляют 10 капель раствора нейтрального ацетата свинца 10% и нагревают до кипения. Моча окрашивается в желто-бурый цвет. Затем добавляют несколько капель аммиака в горячую жидкость в присутствии лактозы появляется типичная красная окраска, а затем ярко красный осадок. Глюкоза дает бледно-розовую окраску и желтоватый осадок.
Лактоза наблюдается главным образом в моче беременной женщины, начиная с 6 месяца беременности или во время кормления грудью или у детей при желудочно-кишечных расстройствах, связанных с молочным питанием.
Мальтоза с фенилгидразином дает в холодном состоянии характерный мальтозазон (рис. 46) в виде почти прямоугольных пластинок, соединенных между собой краями, с температурой плавления = 206°.
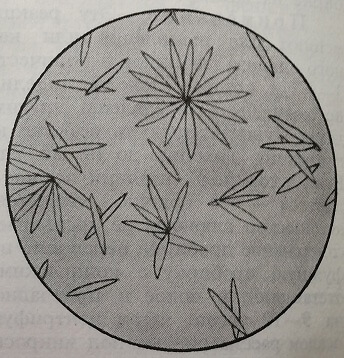
Рис. 46. Кристаллы мальтозазона.
Тест Волька : к 5 мл мочи добавляют 2 мл аммиака и 5 капель раствора едкого натра 22%, затем погружают в водяную баню и подогревают до 70–80°. В присутствии мальтозы или лактозы спустя 2–3 минуты появляется красная окраска.
Левулозу идентифицируют реактивом Селиванова: к 2 мл резорцина и 0,5 мл серной кислоты добавляют 97,5 мл дистиллированной воды.
Реакция: к 2 мл очищенной мочи добавляют 2 мл реактива Селиванова и 4 мл чистой соляной кислоты, затем погружают на 2 минуты в кипящую водяную баню. В присутствии леву лозы тотчас же появляется красная окраска, похожая на цвет смородины. Позднее появление этой окраски не принимается во внимание. Чувствительность реакции доходит до 0,5 г левулозы/л. Левулоза дает тот же озазон, что и глюкоза.
Полисахариды выявляются после гидролиза мочи соляной кислотой, причем восстановительную способность мочи определяют до или после гидролиза; эта способность более значительна в присутствии полисахаридов. Для гидролиза берут 40 мл мочи и 2 мл чистой соляной кислоты и погружают на 10 минут в кипящую водяную ванну, а после охлаждения нейтрализуют едким натром 10% (индикатор – фенолфталеин 1%) после чего, при помощи 1 капли ледяной уксусной кислоты восстанавливают кислую среду.
Пентозы, главным образом – арабинозу, идентифицируют реактивом Биаля: растворяют 0,2 г орцеина в 100 мл чистой соляной кислоты, затем добавляют 4 капли хлористого железа 10%.
В пробирку берут 5 мл реактива Биаля, нагревают до кипения и осторожно добавляют, сливая по стенкам пробирки, 0,5 – 1 мл очищенной мочи, таким образом, чтобы жидкости не смешивались. В присутствии пентозов на границе раздела жидкостей появляется зеленое кольцо.
Гликуроновую кислоту идентифицируют реактивом Толленса: раствор нафторезорцина 1% в спирте 90°. К 5 мл мочи добавляют 1 мл реактива Толленса и 5 мл чистой соляной кислоты, затем погружают на 10 минут в кипящую водяную баню. В присутствии гликуроновой кислоты появляется синяя окраска.
Благодаря своей альдегидной функции, гликуроновая кислота дает при нагревании растворимый озазон (точка плавления = 130–132°); таким образом его можно отделить от озазона глюкозы.
Определение глюкозы
Метод Сеуз, видоизмененный Дениже и Бонансом
Принцип. Глюкоза восстанавливает гидрат меди в недоокись меди, которая удерживается в растворе ферроцианилом калия. Когда весь гидрат меди восстановлен, глюкоза вступает в реакцию с ферроцианидом, давая бурую окраску, указывающую на конец реакции.
Реактивы.
- Реактивы Фелинга I и Фелинга II, приготовленные как было указано при качественном анализе глюкозы.
- Ферроцианид калия 5%.
- Стандартный раствор глюкозы 1%.
Глюкозу высушивают в сушильном шкафу при 105 – 110°, точно отвешивают 1 г и растворяют в дистиллированной воде в мерной колбе на 100 мл. 1 мл этого раствора содержит 10 мг глюкозы. Сохраняют в холодильнике.
Установление фактора: применяемый при определении реактив является смесью, состоящей из 10 мл раствора Фелинга I, 10 мл раствора Фелинга II и 5 мл ферроцианида калия 5%. Фактором реактива является выраженное в граммах количество глюкозы, расходуемое для восстановления этой смеси.
На практике поступают следующим образом. Вышеуказанную смесь берут в колбу Эрленмейра на 100 мл, нагревают до кипения и титруют раствором глюкозы 1 %, добавляемой по каплям, выдерживая смесь в состоянии непрерывного кипения. Реактив изменяет свою окраску, переходя с синего в грязно-зеленый и затем в желтый цвет. Начиная с этого момента глюкозу следует добавлять осторожно, до внезапного появления бурого цвета, при котором отмечается число миллилитров глюкозы 1%, израсходованных для титрования. Если, например, израсходовано 4 мл то количество глюкозы, необходимое для восстановления реактива составляет 40 мг или выраженное в граммах: f = 0,040.
Техника. В колбу Эрленмейра на 100 мл берут те же количеств реактивов, что и для определения фактора и нагревают до кипения. Затем из бюретки добавляют по каплям мочу, очищенную реактивом Куртоца (выдерживая все время смесь в состоянии кипения), до внезапного появления бурой окраски.
п – количество миллилитров мочи, израсходованных для титрования, так как моча была очищена реактивом Куртона 1/10, соответствующую коррекцию производят умножая полученный результат на 1,1 для того, чтобы получить фактическое количество глюкозы. Следовательно, 5,33 х X 1,1 = 5,86 глюкозы/л.
Примечание. Если моча содержит глюкозу в количестве превышающем 5 г/л, то до определения ее необходимо разбавить следующим образом: 1/1, если моча содержит 5–10 г/л глюкозы; 1/5 если моча содержит 10–12 г/л глюкозы; 1/10, если моча содержит более 20 г/л глюкозы. Получаемые результаты умножают на степень разбавления, соответственно на 2, 5 или 10.
Метод Фелинга
Принцип и реактивы те же, что и для качественного анализа глюкозы этим методом.
Техника. В колбу Эрленмейера на 100 мл берут: 10 мл раствора Фелинга I, 10 мл раствора Фелинга II и 20 мл дистиллированной воды. Доводят до кипения и затем титруют очищенной и надлежащим образом разбавленной мочой, которую добавляют по каплям, выдерживая все время в состоянии кипения до тех пор, пока цвет раствора не перейдет в бледно-желтый.
Примечание. Результат умножают на 1,1 или на 2, в зависимости от того была ли моча очищена реактивом Куртона или Патейна, а также в зависимости от степени разбавления.
Метод Бенедикта
Принцип. Такой же, что и для качественного анализа глюкозы этим методом.
Реактив Бенедикта. Растворяют при нагреве 100 г безводного карбоната натрия, 200 г цитрата натрия или калия и 125 роданида калия в 880 мл дистиллированной воды, и затем фильтруют. Отдельно растворяют
18 г сульфата меди в 100 мл дистиллированной воды, и приливают, непрерывно помешивая, к отфильтрованному раствору, после чего добавляют 5г ферроцианида калия, после растворения которого дополняют до 1 000 мл дистиллированной водой.
Техника. В колбу Эрленмейра берут 10 мл реактива Бенедикта, добавляют 10 г кристаллического карбоната натрия или 5 г безводного карбоната и нагревают до кипения, затем титруют подходящим образом разбавленной мочой, выдерживая жидкость в состоянии кипения, до обесцвечивания.
Расчет. 10 мл реактива соответствуют 0,020 г глюкозы.
Метод Ионеску-Матиу
Принцип. В щелочной среде, при нагревании глюкоза восстанавливает феррицианид калия в ферроцианид. Когда все количество феррицианида было восстановлено, первая капля глюкозы вступает в реакцию с индикатором (насыщенный раствор пикриновой кислоты), и окраска раствора переходит с желтого в красный цвет.
Реактивы.
- Раствор феррицианида калия: растворяют 46 г феррицианида калия и 46 г едкого натра в 1 000 мл дистиллированной воды в мерной колбе.
- Насыщенный раствор пикриновой кислоты. Отвешивают 1,2 г чистой пикриновой кислоты, растворяют в 100 мл горячей воды и после охлаждения фильтруют.
- Стандартный раствор глюкозы 5 °/00. Точно отвешивают 5 г чистой глюкозы, высушенной в сушильном шкафу при 105–110° и растворяют в 1 000 мл дистиллированной воды в мерной колбе; 1 мл содержит 5 мг глюкозы. Сохраняют в холодильнике.
Установление фактора. В колбу Эрленмейера на 100 мл берут 10 мл феррицианида калия (1), 10 капель пикриновой кислоты 1,2% (2), и 20 мл дистиллированной воды. Нагревают до кипения и титруют раствором глюкозы 5 °/оо (3), добавляемым по каплям, все время выдерживая смесь в состоянии кипения до тех пор, пока ее окраска перейдет из желтого в красный цвет.
Так же как и при остальных методах, фактором реактива является выраженное в граммах количество глюкозы, необходимое для восстановления этой смеси. Если для титрования израсходовано 10 мл глюкозы, то количество глюкозы, необходимое для восстановления, составляет 50 мг или выраженное в граммах:/= 0,050.
Техника. В колбу Эрленмейера берут те же количества реактивов что и для установления фактора и нагревают до кипения, затем титруют очищенной и подходящим образом разбавленной мочой до тех пор, пока желтый цвет не перейдет в красный.
Патофизиологические изменения. Чаще всего присутствие глюкозы в моче является результатом расстройств глюцидного обмена, причем в этих случаях глюкозурия является симптомом диабета. Во всех случаях, в которых в моче обнаруживается присутствие восстановительных веществ, в первую очередь необходимо установить, идет ли речь о глюкозе или об иных глюцидах (лактоза, мальтоза и др.). После того, как уточняется этот вопрос, анализ мочи следует повторить для того, чтобы установить, не является ли гликозурия случайной (главным образом пищевого происхождения) или появляется постоянно. И наконец определение гликозурии должно сопровождаться определением глицемии, поскольку известно, что выделение глюкозы через мочу происходит только в случае превышения «порога глицемии», среднее значение которого составляет 180 мг/100 мл и что в случае расстройства глюцидного обмена определение глицемии имеет более важное диагностическое значение.
У диабетиков с почечным склерозом и гипертензией, почечный порог увеличивается, в связи с чем могут наблюдаться гиперглицемии в 3 г/л или даже больше, несопровождаемые гликозурией, а в других случаях она является минимальной.
Пищевые гликозурии появляются в период беременности, при гипергиреоидизме, нервных состояниях и др. И наконец, гликозурии можно встретить и при отравлении окисью углерода, хлороформом, стрихнином, морфием и др.




