Определение минеральных соединений в крови
Хлориды
Взятие крови. Кровь берут посредством венозной пункции в локтевой складке, без стаза, непосредственно через иглу, в градуированную центрифужную пробирку на антикоагулянт. Этим последним может служить гепарин или хирудин (10 единиц на 1 мл крови) или смесь равных частей оксалата натрия и оксалата аммония (1 мг на 1 мл крови). После взятия хорошо смешивают для того, чтобы избежать свертывания, причем однако встряхивание не должно быть слишком сильным.
Центрифугирование. Отделение эритроцитов является одной из основных фаз определения, причем следует учесть, что в этой фазе могут возникнуть существенные погрешности. Для того, чтобы избежать любое изменение физиологического распределения хлора между плазмой и кровяными шариками, во первых, необходимо, чтобы во время центрифугирования контактная поверхность кровяные шарики – плазма была минимальной; поэтому следует пользоваться центрифужными пробирками возможно меньшего диаметра. Во вторых, центрифугировать следует немедленно и на большой скорости (4000–5000 об/мин), по меньшей мере, в течение 30 минут для того, чтобы получить полное осаждение красных шариков. На практике, наблюдение за глобулярным объемом ведут каждые 10 минут, причем необходимо остановиться в тот момент, когда новое 10-минутное центрифугирование уже не изменяет отмеченного объема. После центрифугирования производится точный расчет общего объема, глобулярного объема и плазматического объема.
Разделение плазмы и кровяных шариков. Плазма сливается осторожно с помощью тонко вытянутой пипетки Пастера, избегая повторное попадание плазмы на поверхность кровяных шариков для того, чтобы не вызвать смешение. Оставшаяся плазма собирается как можно более полно с помощью полосы фильтровальной бумаги. Затем снова центрифугируют 5–10 минут и с помощью фильтровальной бумаги абсорбируют последние следы плазмы находящиеся над глобулярной массой.
Пипетку закрывают указательным пальцем, а ее конец доводится до дна центрифужной пробирки; затем отсасываются кровяные шарики наружные стенки пипетки тщательно вытираются прежде чем вводить кровяные шарики в сосуд, в котором производят определение.
Примечание: Центрифужная пробирка должна быть отградуирована в десятых долях мл. Точность градуирования проверяется дистиллированной водой, добавляемой из микробюретки. Для определения хлора в сыворотке взятие крови производят обычным способом, оставляют на коагуляцию и затем сыворотку отделяют.
Измененный метод Лаудат
Принцип: для отделения связанного хлора от органических веществ, разлагают последние предварительно кипячением в насыщенном растворе перманганата калия, в присутствии азотной кислоты и нескольких капель пергидрола или перекиси водорода. Затем хлор и хлориды осаждаются в виде хлористого серебра раствором азотно-кислого серебра 0,05 н. в избытке, в присутствии азотной кислоты.
Азотная кислота препятствует осаждению фосфатов и образованию комплексных соединений с серебром. Избыток азотно-кислого серебра 0,05 н. титруется раствором роданида калия или аммония 0,05 н. по реакции:
AgN03 + KSCN = AgSCN + KN03
используя в качестве индикатора раствор железных квасцов. Когда все серебро превращено в роданид серебра (бесцветного) появляется краснооранжевый цвет, благодаря образованию роданида железа, согласно уравнению:
6KSCN + 2NH4Fe(S04)2 = 2Fe(SCN)3 + 3K2S04 + (NH4)2S04
Реактивы.
- Азотно-кислое серебро 0,05 н.
- Чистая азотная кислота (уд. вес – 1,40).
- Насыщенный раствор перманганата калия.
- Насыщенный раствор перманганата калия.
- Железные квасцы 5% (двойной сульфат железа и аммония).
- Роданид калия 0,05 н.
Техника. В колбу Эрленмейера из иенского стекла на 50–100 мл вводят 10 мл дистиллированной воды, затем добавляют 1 мл плазмы, сыворотки, цельной крови или кровяных шариков, отсасываемых пипеткой, как это было указано выше. Эту пипетку хорошо ополаскивают несколько раз, всасывая дистиллированную воду с 2% аммиаком и выдувая промывочную воду на кровяные шарики. Глобулярная масса тщательно гемолизируется, встряхиванием с дистиллированной водой до полного исчезновения сгустков.
Колбу помещают на асбестовое сито и нагревают в вытяжном шкафу на небольшом пламени, при умеренном кипячении, во избежание выброса. Слегка помешивают небольшой стеклянной палочкой. Кипячение, соответственно окисление считается законченным, когда получается прозрачная жидкость, над осадком хлористого серебра и остается устойчивым бурый цвет образовавшейся окиси марганца. В этот момент добавляют осторожно, во избежание выброса, 1–2 капли пергидрола или перекиси водорода
(4) для обесцвечивания. Жидкость образует пену и должна быть обесцветной или в крайнем случае желтоватой с комочками совершенно белого осадка хлористого серебра (ни в коем случае желтого или бурого). Оставляют для охлаждения и добавляют 2,5 мл железных квасцов (5), затем титруют роданидом калия 0,05 н. (6), добавляемым из 5 мл микробюретки, до появления краснооранжевого цвета, который должен оставаться устойчивым в течение 30 секунд. Во время титрования содержание колбы Эрленмейера слегка встряхивают. Делается отсчет и отмечается количество израсходованных для титрования мл роданида.
Общий хлор может быть получен расчетным путем, исходя из определений плазматического и глобулярного хлора.
Таким образом полученное значение более точно, чем то, которое получается при непосредственном определении крови, вследствие затруднений, возникающих при гомогенизации крови в дозируемом образце.
Физиопатологические изменения. Нормальные значения: в сыворотке или плазме: С1 : 345–375 мг/100 мл; NaCl : 570 – 620 мг/100 мл, в кровяных шариках; С1 : 175–200 мг/100 мл; NaCl: 290– 330 мг/100 мл, в цельной крови; С1 : 275–315 мг/100 мл; NaCl : 450–510 мг/100 мл.
Соотношение глобулярный хлор/плазматический хлор == 0,50–0,54.
Довольно часто гипохлоремии наблюдаются в течение пневмонии и туберкулеза. Пониженные значения встречаются также при отравлениях сулемой и при назначении чрезмерных доз ртутных мочегонных препаратов, при которых хлор переходит из крови в ткань.
Гиперхлоремии наблюдаются при анемиях, нефритах, сердечных декомпенсациях, удержании мочи и др.
Увеличение соотношения глобулярный хлор/плазматический хлор свидетельствует о нагрузке кровяных шариков (и вместе с тем и других тканей) хлором, как это бывает при хронических нефритах с повышенной азотемией; эта гиперхлоремия сопровождается ацидозом. Снижение соотношения глобулярный хлор/плазматический хлор до 0,40 указывает разгрузку хлора из кровяных шариков. Эта гипохлоремия может явиться либо следствием недостаточного подвоза хлоридов, либо вследствие избыточного выведения хлора (рвоты, понос). Довольно часто она сопровождается алкалозом и является показанием для назначения лечения рехлорированием.
Безсолевая диета не вызывает гипохлоремии.
Белковый йод
Метод Санделл-Кольтгоффа
Принцип. Связанный с белками йод переводят в йодид прокаливанием с едким калием и отделяют от летучих веществ экстрагирование спиртом.
Реактивы.
- Буфер ацето-уксусная кислота: 56 мл ледяной уксусной кислоты и 118 г ацетата натрия берут в мерную колбу на 1000 мл, растворяют и дополняют до метки бидистиллированной водой.
- Насыщенный раствор сульфата аммония.
- Насыщенный раствор едкого калия. Совершенно насыщенный раствор необходимо промыть спиртом, свободным от йода на разделительной воронке.
- Этиловый спирт 95°. Очищают дистилляцией с едким натром.
- Серная кислота 7 н. Удаление возможных следов йода из серной кислоты производится нагревом до 150–200° в течение 5 часов.
- Сульфат церия 0,005 н. Получают растворяя соответствующее количество сульфата церия и аммония или сульфата церия серной кислотой 1,6 н.
- Мышьяковистая кислота 0,1 н. Соответствующее количество мышьяковистой кислоты растворяют в небольшом количестве раствора едкого натра н. и подкисляют серной кислотой, таким образом, чтобы конечный раствор соответствовал приблизительно серной кислоте 0,001 н.
- Стандартный раствор йодистого калия. Растворяют 261,6 мг йодистого калия в 1 000 мл бидистиллированной воды. 1 мл содержит 400 мг йода. Не более чем 48 часов до употребления приготовляют соответствующие разбавления для того, чтобы получить раствор с 0,08 мг йода/мл.
- Бидистиллированная вода. Приготовляется повторно, дистиллируя обычную дистиллированную воду в присутствии едкого натра.
Техника.
а) Отделение белкового йода. В центрифужную пробирку вводят 2 мл плазмы, 6 мл буферной ацетоуксусной кислоты (1) и 10 капель насыщенного раствора сульфата аммония (2). Пробирку помещают на 10 минут в кипящую водяную баню, непрерывно помешивая, чтобы предупредить осаждение крупных, трудно смываемых хлопьев. Осадок, содержащий « гормональный йод» отделяется центрифугированием и трижды промывается по 6 мл бидистиллированной воды для удаления неорганического йода.
б) Разрушение органических веществ. К промытым белкам добавляют 2 мл насыщенного раствора едкого калия (3), затем пробирку ставят в кипящую водяную баню до растворения белков. Получаемая паста количественно переводится с дистиллированной водой в никелевый тигель, подогреваемый на небольшом пламени, до прекращения вспенивания.
Для удаления газов тигель ставят в муфельную печь и нагревают в течение 15 минут при 250°. К концу температура медленно повышается до 380°, уровень, на котором выдерживается в течение 10 минут.
в) Экстрагирование. Расплавленная в тигеле масса растворяется в очень малом количестве воды, а после выпарки до пастообразной консистенции экстрагируется 5 мл этилового спирта, который затем сливается в другой никелевый тигель. Экстрагирование повторяется трижды по 2 мл спирта. Спирт выпаривают, а тигель нагревают в течение 15 минут при 500–550°.
г) Определение йода. Осадок растворяют в бидистиллированной воде, затем фильтруют в мерную колбу на 50 мл, споласкивая несколько раз тигель и фильтр. До колориметрирования добавляют 2 мл серной кислоты 7 и (5), встряхивают до прекращения бурного выделения газа и доводят до метки. Определение затухания, соответствующего времени полураспада церия производится наливая в одну из кювет фотометра Пульфриха воду, а в другую – раствор состоящий из 0,5 мл сульфата церия 0,05 н. 6 и 23,5 мл воды.
Отсчитывается затухание. Для определения времени полураспада образца в кювету берут: 20 мл раствора из мерной колбы, 1 мл бидистиллированной воды, 2 мл мышьяковистой кислоты 0,1 н. (7) и 1 мл сульфата церия 0,05 н., после чего время измеряют с помощью хронометра, который пускают в момент добавления сульфата церия и останавливают в момент, когда наблюдается одинаковый оттенок обоих полукругов, причем барабан соответствующий кювете с образцом расположен на делении соответствующем половине взятого количества церия; это деление устанавливается предварительно, как было указано выше. Отсчет точно повторяется с другими 20 мл образца, к которым добавили 1 мл стандартного раствора йода.
Нормальное значение. В нормальных условиях плазматический йод колеблется в пределах от 4 до 8 мг на 100 мл.
Фосфор
В организме фосфор находится в виде неорганических и органических производных фосфорных кислот. Кровь содержит буферную систему, состоящую из моно- и динатриевого фосфата, который наряду с бикарбонатами способствует поддержанию постоянной концентрации водородных ионов органически связанная фосфорная кислота находится в бесчисленном множестве веществ, а именно в тех, которые в результате интенсивных биологических превращений являются решающими для явления жизни как таковой.
Среди этих последних следует отметить: сложные фосфорные эфиры (дифосфоглицериновый, гексозофосфаты, глицерофосфаты, фосфаты, компоненты нуклеиновых кислот, принимающих участие в структуре клеточных ядер и являющихся материальной основой наследственных характеристик), липидный фосфор (фосфатиды, лецитины, цефалины и др.)
Неорганический фосфор (минеральный)
Метод Белля, Дуази, Бриггса
Принцип. Ион РО4 дает с молибдатом аммония в кислой среде фосфомолибдат аммония, который в результате восстановления гидрохиноном и сульфитом натрия переходит в молибден синий. Синий цвет пропорционален количеству молибдена в фосфомолибдате, и следовательно количеству фосфора. Он сопоставляется колориметрически с цветом стандартного раствора фосфата.
Реактивы.
- Трихлоруксусная кислота 20%.
- Молибдат аммония. Отвешивают 25 г молибдата аммония для анализа, растворяют в 300 мл дистиллированной воды, фильтруют, переводят в мерную колбу на 500 мл, осторожно добавляют 75 мл концентрированной серной кислоты, а после охлаждения дополняют до метки дистиллированной водой.
- Сульфит натрия 20%. Приготовляется в момент употребления в небольших количествах.
- Гидрохинон 0,5% с 1 каплей концентрированной серной кислоты. Хранится в темноте в бурой бутылке. Раствор должен быть бесцветным, а если по истечение некоторого промежутка времени он приобретает желто-коричневый цвет, необходимо приготовить другой свежий раствор.
- Стандартный раствор монокалиевого фосфата. Отвешивают 0,4394г монокалиевого фосфата «по Сёренсену», предварительно высушенного в эксикаторе, переводят в мерную колбу на 1000 мл, растворяют и дополняют дистиллированной водой до метки. Для консервирования добавляют несколько капель хлороформа: 1 мл = 0,1 мг фосфора. Из этого раствора готовят необходимые разбавления для построения калибровочной кривой на фотоколориметре Пульфриха. В момент употребления приготовляется рабочий стандарт, для чего берут 10 мл стандартного раствора, точно отмеренного в мерную колбу на 100 мл и разбавляют дистиллированной водой до метки.
Техника.
а) Дезальбуминирование. Берут 2 мл сыворотки или цельной крови, добавляют 6 мл дистиллированной воды и 2 мл трихлоруксусной кислоты 20%. Хорошо встряхивают, оставляют в покое на 10 минут и затем фильтруют.
б) Появление окраски. В мерную колбу (или градуированную пробирку) на 10 мл наливают 5 мл прозрачного фильтрата (1 мл сыворотки), 1 мл молибдата аммония (2), 1 мл сульфита натрия 20% (3) и 1 мл гидрохинона 0,5% (4). Одновременно приготовляется контрольный образец с 2 мл стандартного раствора (0,2 мг фосфора) и 3 мл трихлоруксусной кислоты 20% (1) вместо фильтрата, затем добавляют остальные реактивы.
Обе колбы или пробирки дополняют до 10 мл дистиллированной водой, слегка встряхивают и спустя 20 минут производится сравнение окрасок на колориметре Дюбоска или оптическая плотность анализируемого образца (затухание) отсчитывается на фотометре Пульфриха с желтым фильтром на 570 мА и кюветой на 10 мм.
Примечания. Для восстановления фосфомолибдата аммония бисульфит натрия и гидрохинон можно заменить 1 мл раствора аскорбиновой кислоты 1% в соляной кислоте 0,1 н.
Неорганический фосфор равномерно распределяется между эритроцитами и плазмой. В крови органического фосфора почти в 10 раз больше, чем количество неорганического. По этой причине в свеже взятой крови в течение первых 2–3 часов органическая кислоторастворимая фракция может увеличиваться за счет неорганического фосфора. По истечении этого промежутка времени происходит обратное явление: кислоторастворимый органический фофсор подвергается гидролизу, с образованием неорганического фосфора. В гемолизированной крови этот гидролиз происходит немедленно и весьма интенсивно.
Следовательно, при взятии крови для определения фосфора необходимо избегать гемолиза, а определение следует производить тотчас же после взятия.
Общий кислоторастворимый фосфор
Метод Белля, Дуази, Бриггса
Принцип. В результате минерализации в колбе Кьельдаля органические вещества уничтожаются серной кислотой и азотной кислотой, причем фосфор переводится в неорганическую форму. Затем определение производят по вышеописанному способу.
Реактивы.
- Чистая концентрированная серная кислота без фосфора.
- Чистая концентрированная азотная кислота без фосфора.
- Реактивы указанные для предыдущего способа.
Техника.
а) Дезальбуминирование. К 2 мл сыворотки или 1 мл цельной крови добавляют 6 мл дистиллированной воды (для крови 7 мл) и 2 мл трихлоруксусной кислоты 20%. Хорошо встряхивают, оставляют в покое на 10 минут, затем фильтруют.
Минерализация. В колбу Кьельдаля на 25 мл вводят 5 мл прозрачного трихлоруксусного сывороточного фильтрата крови. В другую колбу Кьельдаля наливают фосфат (0,50 мл фосфора). В обе колбы добавляют 10 капель концентрированной серной кислоты (1) и 2–3 стеклянные бусинки. Колбы ставят в вытяжной шкаф, непосредственно на небольшое пламя, на высоте 1 –1,5 см от пламени и слегка подогревают до кипения, наблюдая затем, чтобы жидкость не выплескивалась наружу. Продолжают умеренное кипячение, до появления паров триокиси серы с характерным резким запахом. В этот момент горелки удаляют, оставляют для охлаждения и добавляют по 1 мл концентрированной азотной кислоты и снова кипятят, причем минерализация продолжается до тех пор, пока не прекращается выделение окислов азота, а жидкость не становится совершенно обесцвеченной или имеет только бледно-желтый оттенок. Если жидкость имеет бурый цвет, снова добавляют несколько капель концентрированной азотной кислоты и затем продолжают кипятить до обесцвечивания.
После охлаждения содержание переводят в мерные колбы на 10 мл, споласкивают колбы Кьельдаля три раза по 1–2 мл дистиллированной воды, добавляя промывную воду в мерные колбы, доводят до метки.
Из этих жидкостей берут 5 мл (0,5 мл сыворотки или 0,1 мл крови) и затем обрабатывают так же как и при определении неорганического фосфора.
Примечания. Если из полученного значения вычесть неорганический фосфор, то получают значения кислоторастворимого органического фосфора.
Метод Дениже
Принцип. Тот же, что и для метода Белля, Дуази, Бриггса, лишь стой разницей, что восстановление фосфомолибдата аммония в синюю окись молибдена производится посредством раствора хлористого олова.
Реактивы.
- Концентрированная азотная кислота.
- Концентрированная серная кислота.
- Этиловый спирт 95%.
- Сульфмолибденовый реактив. К 100 мл раствора молибдатааммония 10% осторожно добавляют равный объем концентрированной серной кислоты.
- Хлористое олово. В пробирку берут 0,10 г олова в виде тонких листов (оловянная бумага) или небольших гранулей и добавляют 2 мл концентрированной соляной кислоты и 1 каплю раствора сульфата меди 4%. Слегка нагревают до полного растворения, охлаждают, а объем дополняют дистиллированной водой до 10 мл. Если на дне образуется осадок, прозрачную часть, являющуюся рабочим реактивом, сливают. Этот раствор остается устойчивым не более 1 недели.
- Стандартный раствор фосфора (1 мл = 0,01 мг) приготовляют так же, как при методе Белля, Дуази, Бриггса.
Техника.
а) Минерализация. В фарфоровую чашку диаметром 8 –10 см вводят 1 мл цельной крови, затем добавляют слегка помешивая 1 мл азотной кислоты (1), 1 мл серной кислоты (2) и 2 мл этилового спирта (3) по каплям. Происходит бурное выделение газов, по прекращении которого чашечку покрывают стеклянной воронкой немного меньшего диаметра, таким образом, чтобы она погрузилась в чашку примерно на 1 см. Чашку ставят на песочную баню в вытяжной шкаф и слегка нагревают до исчезновения желто-бурых паров окислов азота и появления белых паров триокиси серы с едким запахом, причем осадок в чашке имеет бурокоричневый цвет. В этот момент горелку удаляют, воронку снимают и добавляют 1 каплю азотной кислоты, затем снова закрывают воронкой и продолжают нагревать для повторного окисления азотной кислотой. Цикл этих операций продолжается до окончательного обесцвечивания массы в чашке (бледножелтый оттенок), после чего нагрев продолжают до обильного выделения белых паров. Затем оставляют для охлаждения, добавляют 10–12 мл дистиллированной воды и нагревают до кипения, причем кипячение продолжается до тех пор, пока объем не уменьшится на половину. Эта операция является необходимой для гидролиза мета- и пирофосфорных ионов, возникающих в сернокислотной среде, которые нельзя идентифицировать посредством молибденового реактива. После этого оставляют для охлаждения и объем дополняют до 200 мл дистиллированной воды.
б) Получение окраски. В пробирку наливают 5 мл (0,025 мл крови) из таким образом разбавленной жидкости и добавляют 4 капли сульфомолибденового реактива (4) и 2–4 капли хлористого олова (5), затем слегка взбалтывают. В другую пробирку берут 5 мл стандартного раствора (0,05 мг фосфора) и добавляют те же реактивы. Спустя 10 минут окраски сопоставляются на колориметре или затухание анализируемого образца отсчитывается на фотометре Пульфриха.
Примечания. Метод отличается высокой чувствительностью и дает возможность определять до 0,2 (гг фосфора/100 мл.
Так же, как в случае вышеописанных способов пропорциональность между концентрацией фосфора и интенсивностью получаемой синей окраски не является абсолютно точной.
Метод Машбеф-Дельсаля
Принцип. Тот же, что и для метода Белля, Дуази, Бриггса.
Реактивы.
- Чистая концентрированная серная кислота без фосфора.
- Чистая концентрированная азотная кислота без фосфора.
- Реактивы (2), (3), (4) и (5), применяемые при способе Белля, Бриггса.
Техника.
а) Минерализация. В колбу Кьельдаля на 25 мл берут 1 мл цельной крови или 2 мл сыворотки и добавляют 2–3 стеклянные бусинки и 1 мл серной кислоты (1). Колбу устанавливают в наклонном положении и осторожно доводят до легкого кипения с помощью небольшого пламени (микрогорелка) в вытяжном шкафу. Спустя 1 минуту оставляют для охлаждения, добавляют 1 мл азотной кислоты (2) и снова доводят до кипения. Если пары окислов азота полностью выделились, а жидкость в колбе имеет бурую окраску, добавляют несколько капель азотной кислоты и продолжают разрушение, повторяя добавление азотной кислоты в случае необходимости, до полного обесцвечивания жидкости, которая в крайнем случае должна иметь слабый желтый оттенок.
б) Получение окраски. После охлаждения объем находящейся в колбе жидкости дополняют до 6 мл дистиллированной водой, после чего колбу Кьельдаля помещают на 15 минут в кипящую водяную баню. Охлаждают до температуры лаборатории, затем добавляют 2 мл молибдата аммония 5% (2), 1 мл сульфита натрия 20% (3) и 1 мл гидрохинона 0,5% (4). В другую колбу Кьельдаля наливают 2 мл стандартного раствора (5) (0,02 мг фосфора) и добавляют 4 мл дистиллированной воды и те же количества реактивов. Через 30 минут окраски сопоставляются на колориметре Дюбоска или оптическая плотность анализируемого образца отсчитывается на фотометре Пульфриха с желтым фильтром на 570 мц и кюветой на 5 или 10 мм.
Липидный фосфор (лецитин)
Принцип. Извлечение липидов из крови со смесью равных частей спирта и эфира. После минерализации экстракта липидный фосфор определяется способом Белля, Дуази, Бриггса.
Реактивы.
- Смесь равных частей спирта и эфира.
- Серная кислота ОД н.
- Пергидрол.
- Реактивы для способа Белля, Дуази, Бриггса, за исключением трихлоруксусной кислоты.
Техника.
а) Извлечение липидов. В мерную колбу на 25 мл наливают 18 мл спиртно-эфирной смеси (1), затем добавляют 0,5 мл сьшоротки или плазмы. Хорошо встряхивают и помещают на электрическую водяную баню в вытяжном шкафу до тех пор, пока смесь не начнет кипеть. В этот момент ее вынимают из бани, охлаждают до температуры лаборатории, дополняют до метки спиртно-эфирной смесью, хорошо встряхивают и фильтруют.
б) Минерализация. 5 мл фильтрата (0,1 мл сыворотки) переводят в колбу Кьельдаля на 25 мл, затем добавляют 0,5 мл серной кислоты 0,1 н. (2) и 2–3 стеклянные бусинки. Нагревают до кипения на микрогорелке в вытяжном шкафу, причем колбу ставят в наклонном положении. Когда содержание колбы окрашивается в бурый цвет, его охлаждают и затем добавляют 1 каплю пергидрола (3), продолжая кипячение и в случае необходимости повторяя добавление пергидрола до тех пор, пока раствор не станет бесцветным. После охлаждения объем дополняют дистиллированной водой до 10 мл.
в) Получение окраски. Из вышеуказанной жидкости берут 5 мл (0,05 мл сыворотки) и производят определение неорганического фосфора методом Белля, Дуази, Бриггса, учитывая при расчете степень разбавления сыворотки (1/20), а также и то обстоятельство, что липидный фосфор составляет около 4% из лецитина. Следовательно: лецитин мг/100 мл = неорганический фосфор мг/100 мл X 25.
Физиопатологические изменения. У здоровых людей фосфор имеется в следующих количествах:
Неорганический фосфор в сыворотке: у взрослых 3–4 мг/100 мл; у детей 4–6 мг/100 мл.
Этерифицированный фосфор в сыворотке: у взрослых 2–5 мг/100 мл; у детей 4–7 мг/100 мл.
Общий кислоторастворимый фосфор: в сыворотке 2,5–5 мг/100 мл; в крови 18–38 мг/100 мл.
Липидный фосфор: в сыворотке 6–7 мг/100 мл; в крови 12–14 мг/100 мл.
Общий фосфор: в сыворотке 7–15 мг/100 мл; в крови 30–50 мг/100 мл.
Летом эти значения несколько выше, чем зимой. В нормальных условиях фосфор слегка снижается во время дигестии глюцидов. Так, например, спустя 30 минут после приема 100 г глюкозы, количество фосфора в сыворотке снижается на 1–1,5 мг/100 мл. Восстановление исходного значения наступает через 4–5 часов.
Количество фосфора понижено при рахитизме (параллельно уровню кальция), размягчении костей, гиперпаратиреоидизме и гиперинсулинизме.
Гиперфосфатемии встречаются в период спаивания переломов, прц удержании мочи в течение нефритов, гипопаратиреоидизме, сочетаниях, а также при гиперавитаминозах D и облучениях ультрафиолетовыми лучами при лечении рахитизма. В этом случае определение фосфора может служить для контроля лечения.
При анемии количество липидного фосфора увеличивается в эритроцитах и снижается в сыворотке. Фосфор сывороточных липидов повышается при диабете, нефритах, патологической беременности и определенных случаях расстройства печеночной функции, при острой лейкемии наблюдается снижение липидного и органического фосфора.
Сера
Кровь содержит приблизительно 140 мг общей серы на 100 мл в двух формах: белковая сера (в сульфидированных аминокислотах белков крови, как например, метионин и цистин) и небелковая сера, в которой Лёплер и сотрудники различают окисленную серу, соответствующую минеральным или органическим сульфатам и серным сложным эфирам или сульфонированным производным и нейтральная сера, состоящая из сульфидированных производных тиоловой группы (SH). Окисленная сера составляет примерно 80% небелковой серы. Для клинических нужд обычно определяются: общая сера, небелковая сера и окисленная сера, а остальные формы серы определяются в виде разницы.
Общая сера
Принцип. После минерализации нитро-перхлорной кислотой сера осаждается в виде сульфата бензидина, образующего вследствие гидролиза серную кислоту, причем эта последняя титруется едким натром 0,02 н.
Реактивы.
- Нитроперхлорная кислота. Смешивают 3 объема чистой азотной кислоты 40° В с 1 объемом чистой перхлорной кислоты (уд. вес = 1,615).
- Бромфенол синий, спиртовый раствор 0,04%.
- Едкий натр.
- Соляная кислота 0,1 н.
- Едкий натр 0,02 н.
- Чистый ацетон.
- Бензидин растворенный в воде подкисленной соляной кислотой (реактив Фиске). Навеску 4 г бензидина, очень тонко размельченного в ступке, взвешивают в 150 мл дистиллированной воды в мерной колбе на 250 мл, после чего небольшими количествами при непрерывном встряхивании добавляют небольшими порциями 50 мл соляной кислоты н. Бензидин растворяется тотчас же, а если остаются несколько комков, то их размельчают с помощью стеклянной палочки с наконечником в виде резинового кольца. Хорошо встряхивают и дополняют дистиллированной водой до метки. Раствор сохраняют в бурой бутылке в темном месте, причем в этих условиях раствор пригоден не менее 8 месяцев.
- Ацетон с 10% воды.
- Смесь равных частей спирта и эфира.
- Бромтимол синий, спиртовый раствор 0,04%.
Техника.
а) Минерализация. В колбу Кьельдаля на 25 мл берут 2–3 стеклянные бусинки и с помощью пипетки отмеривают 1 мл сыворотки и 10 мл нитро-перхлорной кислоты (1). Колбу устанавливают в наклонном положении в вытяжном шкафу, после чего проводят умеренное кипячение. Слегка бурая жидкость становится желтой и под конец становится прозрачной. Во время кипячения выделяются обильные пары перхлорной кислоты. Кипячение продолжается примерно 45 минут, – промежуток времени необходимый для испарения жидкости из колбы Кьельдаля. Кипячение прекращают когда вся жидкость исчезла из нижней сферы, причем на стенках остались только пары, тотчас же конденсирующиеся после прекращения нагрева.
б) Осаждение серы. После охлаждения к осадку добавляют 7–8 дистиллированной воды, споласкивая колбу Кьельдаля 2–3 раза небольшим количеством дистиллированной воды. Добавляют 1 каплю бромфенола синего (2) и затем по каплям едкий натр (3), пока не появится зеленовато-синий или синий оттенок (pH более 3). Слегка подкисляют, добавляя по капле соляную кислоту 0,1 н. (4) до желтого цвета, после чего снова приводят к бледно-синему цвету, добавляя по капле едкий натр 0,02 н. (5). Затем добавляют 8 мл ацетона (6) и 2 мл бензидина (7). Получается pH около 2,8. Оставляют в покое на 5 минут, затем фильтруют на пористом фильтре из иенского стекла G4, присоединенном к водоструйному или вакуум насосу. Осадок промывают 4 раза по 2 мл ацетона (8) и 1 раз спиртово-эфирной смесью (9), осторожно споласкивая стенки фильтра, а в заключение споласкивают струей дистиллированной воды.
в) Гидролиз сульфата бензидина. Фильтрат переводят в стакан Берзелиуса на 250 мл, заливают дистиллированной водой и кипятят в течение 15 минут.
г) Титрование выделенной гидролизом серной кислоты производится при кипячении, добавляя 4 капли бромтимола синего (10), затем из микробюретки (с делениями в десятые доли мл) добавляют по капле едкий натр 0,02 н. до появления бледно-голубой окраски.
Расчет. Общая сера мг/100 мл = 30 X п, где: п – количество мл едкого натра 0,02 н., израсходованных для титрования.
Небелковая сера
Нефелометрический метод
Принцип. После дезальбуминирования серу осаждают хлоридом бария в виде сульфата бария, который определяют нефелометоически на фотометре Пульфриха.
Реактивы:
- Трихлоруксусная кислота 20%.
- Едкий натр 2 н.
- Желатина-хлористый барий.
- Сульфат калия, стандартный раствор.
- Калибровочную кривую строят используя серию стандартных растворов, содержащих: 0,01; 0,02; 0,03; 0,04; 0,06 и по 0,10 мг серы/мл.
Берут по 2 мл из каждого разбавления, добавляют 3 мл дистиллированной воды и 1 мл желатины-хлористого бария (3). Слегка встряхивают, после 30 минут отсчитывают и записывают оптическую плотность, соответствующую каждому разбавлению на фотометре Пульфриха, с синим фильтром L3 и кюветой на 10 мл.
Техника.
а) Дезальбуминирование. В пробирку наливают 4 мл сыворотки и добавляют 4 мл трихлоруксусной кислоты 20% (1). Хорошо встряхивают и через несколько минут фильтруют или центрифугируют на больших оборотах (3500–4000 об/мин.).
б) Осаждение серы.4 мл фильтрата (2 мл сыворотки частично нейтрализуют, добавляя 1 мл едкого натра 2 н. (2). Затем проверяют pH раствора, который должен соответствовать примерно 2,8 и добавляют 1 мл раствора желатины-хлористого бария (3). По истечении примерно 30 минут определяется оптическая плотность на фотометре Пульфриха с синим фильтром L3 и кюветой на 10 мм, после чего небелковую серу подсчитывают по отношению к калибровочной кривой.
Окисленная сера
Принцип. После дезальбуминирования и гидролиза серной кислотой серу осаждают хлористым барием в виде сульфата бария, определяемого нефелометрически.
Реактивы.
- Соляная кислота н.
- Едкий натр 2 н.
- Реактивы используемые для определения небелковой серы.
Техника.
а) Дезальбуминирование. К 4 мл сыворотки добавляют 4 мл трихлоруксусной кислоты 20%. Хорошо встряхивают и через несколько минут фильтруют.
б) Гидролиз соляной кислоты. В колбу Эрленмейера не 50 мл с обратным холодильником наливают 4 мл трихлоруксусного фильтрата, 2 мл сыворотки и 2 мл соляной кислоты н. (1). Кипятят 15 минут, причем воду пропускают через холодильник только после того, как объем жидкости сократился до 2–3 мл. После охлаждения жидкость переводят в градуированную пробирку, споласкивая колбу 1 мл едкого натра 2. Но затем небольшим количеством дистиллированной воды, таким образом, чтобы конечный объем вместе с промывочными жидкостями равнялся точно 5 мл.
в) Определение производится на этих 5 мл жидкости (2 мл сыворотки) (по способу описанному для определения небелковой серы).
Физиопатологические изменения. Нормальные значения: общая сера в сыворотке – 120–170 мг/100 мл; небелковая сера в сыворотке – 5–9 мг/100 мл; окисленная сера в сыворотке – 4–7 мг/100 мл.
Небелковая сера подвергается физиологическим колебаниям, особенно под влиянием питания. Она снижается в период соблюдения вегетарианского режима, увеличиваясь уже через несколько часов после обильного поглощения мясной пищи. Кроме того небелковая сера увеличивается во время беременности.
Небелковая сера повышается при инфекционных легочных болезнях, пневмониях, гнойном плеврите и др., в течение которых она может достичь 20–37 мг на 100 мл. При хронических нефритах рост еще более значителен, причем он может достичь 40–60 мг/100 мл. Окисленная сера снижается при тяжелых инфекционных состояниях, асистолических кардиопатиях, при отравлении бензолом, а также при некоторых заболеваниях печени, как например, желтухе или при ряде заболеваний надпочечных желез, как например, болезнь Аддисона.
Натрий
Колориметрический метод
Принцип. После дезальбуминирования натрий осаждают в виде тройного ацетата уранила, магния и натрия (соль Штренга). Этот последний обрабатывается раствором ферроцианида калия в уксусной среде и дает бурую окраску, которую можно колориметрировать.
Реактивы.
- Трихлоруксусная кислота 20%.
- Реактив Кагане: растворяют на горячей водяной бане 32 г ацетата урана и 100 г ацетата магния в смеси состоящей из 20 мл ледяной уксусной кислоты, 500 мл спирта 90° и 300 мл дистиллированой воды, охлаждают и объем дополняют до 1 000 мл. Оставляют в покое на 24 часа. Реактив сохраняют в темноте не более 1 месяца, и вследствие того, что он постоянно дает осадок, фильтруют перед употреблением.
- Спирт 95°.
- Титрованный раствор ацетата уранила, магния и натрия: 20 мл 2,5% раствора хлористого натрия осаждают 500 мл реактива Кагане. Оставляют в покое на 30 минут, затем фильтруют через воронку Бюхнера, соединенную с водоструйным насосом. Осадок промывают три раза реактивом Кагане и 3 раза спиртом 90°. Высушивают в течение 1 часа в сушильном шкафу при 105°. Точно отвешивают 1 г сухого осадка в эксикаторе, затем растворят в 1000 мл дистиллированной воды в мерной колбе: 1 мл раствора содержит 0,015 мг натрия.
- 1% ферроцианид калия, к которому после растворения добавляют 1 мл ледяной уксусной кислоты. Приготовляют в момент употребления.
Техника.
а) Дезальбуминирование. В пробирку наливают 2 мл негемолизированной сыворотки, добавляют 2 мл трихлоруксусной кислоты 20% (1), хорошо встряхивают и фильтруют.
б) Осаждение натрия. В центрифужную пробирку отмеряют 1 мл прозрачного фильтрата (0,5 мл сыворотки) и 7 мл реактива Кагая(2) , слегка встряхивают и оставляют в покое на 30 минут. Центрифугируют на высоких оборотах (4 000–5 000 об/мин) для того, чтобы весь осадок собрался на дне пробирки. Надосадочную жидкость удаляют сифонированием, а осадок промывают дважды по 5 мл реактива Кагане и трижды по 5 мл спиртом 95° (3). После каждого добавления промывочной жидкости хорошо центрифугируют, затем надосадочную жидкость удаляют сифонированием. К концу осадок растворяют в 2 мл дистиллированной воды и переводят в градуированную пробирку на 10 мл, споласкивая несколько раз центрифужную пробирку и добавляя промывочную воду в градуированную пробирку. Объем жидкости доводят точно до 10 мл и хорошо смешивают. Если образуется осадок фосфата урана – фильтруют.
в) Получение окраски. Из прозрачного фильтрата берут 5 мл (0,25 мл сыворотки) в пробирку. В другую пробирку берут 5 мл стандартного раствора тройного ацетата (4). В обе пробирки добавляют по 5 мл уксусного раствора ферроцианида (5) и 3 мл дистиллированной воды. Спустя 30 минут окраски сопоставляют на колориметре Дюбоска.
Калий
Комплексометрический метод
Принцип. Осаждение калия гексакобальтонитритом натрия (реактив Краммер – Тисдаля) в виде гексакобальтонитрита калия и натрия.
Из этого соединения выделяется кобальт, который затем титруют ЭДТА (двухнатриевая соль этилендиаминотетрауксусной кислоты) в присутствии мурексида в качестве индикатора.
Реактивы:
- Раствор гексакобальтонитрита натрия. а) Растворяют 25 г нитрата кобалта в 50 мл дистиллированной воды, затем добавляют 12,5 мл уксусной кислоты; б) растворяют 120 г нитрита натрия в 180 мл дистиллированной воды, слегка нагревая на водяной бане.
После охлаждения все количество раствора а смешивают с 210 мл раствора б затем водоструйным насосом через раствор барботируют струю воздуха с небольшой скоростью до тех пор пока не перестают выделяться бурые пары окислов азота (2–3 часа). В этот момент запах паров окислов азота исчезает, а жидкость, которая вначале была темнобурого цвета, приобретает более светлую окраску и становится прозрачной. Реактив сохраняют в холодильнике в бурой бутылке с притертой пробкой, не более одного месяца. Перед употреблением фильтруют. - Нормальный раствор соляной кислоты.
- Чистая мочевина, кристаллическая.
- Раствор чистого аммиака 2 н.
- Индикатор мурексид (пурпурат аммония). Используют тонко размельченную смесь мурексида и хлористого натрия в соотношении 1/200.
- Раствор ЭДТА 0,001 н. Растворяют 0,186 1 г в 1000 мл дистиллированной воды в мерной колбе.
Техника. Наливают 1 мл негемолизированной сыворотки в центрифужную пробирку, добавляют по каплям 2 мл раствора гексакобальтонитрита натрия (1), затем сверху осторожно добавляют 1 мл дистиллированной воды. Оставляют на три часа в холодильнике, затем центрифугируют 10 минут при 3000 об/мин.
Надосадочную жидкость отсасывают сифонированием, затем осадок трижды промывают дистиллированной водой (со льда), центрифугируя и удаляя промывочную воду. Промывочную воду вводят осторожно для того, чтобы не нарушить осадок. После последнего промывания пробирку переворачивают отверстием вниз и кладут на фильтровальную бумагу для стечения остатка жидкости, затем осадок растворяют в 1 мл соляной кислоты н. (2). Добавляют щепотку (несколько сантиграммов) кристаллов мочевины (3) и пробирку помещают в кипящую водяную баню. Помешивают тонкой стеклянной палочкой, до тех пор пока жидкость не станет бесцветной, затем охлаждают.
Добавляют 5 мл аммиака 2 н. (4) и щепотку индикатора (5), после чего титруют раствором ЭДТА 0,001 н. (6) до сине-фиолетового цвета.
Параллельно титруют слепой образец, используя вместо сыворотка дистиллированную воду. Значение полученного при титровании контрольного образца (nj) вычитают из значения анализируемого образца (п).
Расчет. 1 мл раствора ЭДТА 0,00 1 н. соответствует 0,078 2 мг калия.
Калий мг/100 мл = (п–пг) X 0,0782 X 100.
Примечания. Имея ввиду, что сыворотка содержит в 10 раз больше количества калия по сравнению с эритроцитами, кровь следует брать избегая гемолиз (взятие должно производиться сухой иглой, непосредственно в центрифужную пробирку, хорошо высушенную). Тотчас же после взятия крови, пробирку вводят в термостат при 37° для коагуляции, затем с помощью тонкой стеклянной палочки осторожно отделяют верхний край сгустка, приставшего к стенкам пробирки, стараясь не разрушить его. После отделения сыворотки, немедленно центрифугируют, отсасывая сыворотку и приступая к проведению анализа. В случае сохранения сыворотки на сгустке, калий диффундирует из эритроцитов в сыворотку, что влечет за собой значительную ошибку, которая тем больше, если сыворотка гемолизирована. Определение калия производится немедленно. Сыворотку не сохраняют продолжительное время, так как при консервировании может выделяться аммиак, который с гексакобальтонитритом натрия дает нерастворимый осадок, завышающий результат определения.
Колориметрический метод Гоффман-Якобса
Принцип. Осаждение калия гексакобальтонитритом натрия в виде кобальтонитрита калия и натрия, который с ферроцианидом натрия дает зеленую окраску, пропорциональную количеству калия, присутствующего в анализируемом образце. Окраска сопоставляется колориметрически с окраской стандартного раствора известной концентрации.
Реактивы.
- Реактив Краммер – Тисдаля: а) Растворяют 5 г нитрата кобальта в 10 мл дистиллированной воды. б) Растворяют 30 г нитрита натрия в 45 мл дистиллированной воды. Раствор (а) смешивают с 42 мл раствора (б). Через жидкость барботируют сильную струю воздуха до тех пор, пока не прекращается выделение бурых паров окислов азота (около 30 минут). Реактив можно сохранять в бутылке темного цвета в холодильнике не более двух недель. Если в течение этого времени цвет раствора темнеет, через него снова пропускают струю воздуха. Перед употреблением фильтруют.
- Спирт 70%.
- Хлоргидрат холина 1%.
- Ферроцианид натрия 2%.
- Стандартный раствор кристаллического сульфата калия для анализа. Точно отвешивают 0,228 г сульфата калия, переводят в мерную колбу на 500 мл, растворяют в дистиллированной воде и дополняют до метки. 1 мл содержит 0,2 мг калия.
Техника.
а) Осаждение калия. В градуированную центрифужную пробирку из иенского стекла берут 1 мл негемолизированной сыворотки добавляют 2 мл стандартного реактива Краммера-Тисдаля (1). В другую пробирку берут 1 мл стандартного раствора (5), который обрабатывают так же, как и анализируемый образец, причем этот стандартный раствор служит для сравнения. Обе пробирки оставляют в покое на один час для полного осаждения. Затем добавляют по 1 мл дистиллированной воды, встряхивают и центрифугируют 5 минут на больших оборотах (3 500–4 000 об/мин.).
Надосадочную жидкость осторожно удаляют сифонированием, затем центрифужные пробирки кладут отверстием вниз на фильтровальную бумагу для стечения остатка жидкости. Спустя 2–3 минуты, осадок промывают 2 мл дистиллированной воды со льда, затем 5 мл спирта 70% (2). После добавления промывочной жидкости тщательно центрифугируют, затем надосадочную жидкость удаляют сифонированием, а пробирки кладут отверстием вниз на фильтровальную бумагу для стечения остатка жидкости.
б) Получение окраски. К осадку в пробирки добавляют 2 мл дистиллированной воды и растворяют погружая пробирки на 2–4 минуты в кипящую водяную баню. Затем добавляют по 0,5 мл хлоргидрата холина 1% (3) и 0,5 мл ферроцианида натрия 2% (4) и дополняют объем точно до 4 мл дистиллированной водой. Оба цвета сравниваются на колориметре Дюбоска. Окраска устойчива в течение нескольких часов.
Примечание. Колориметрический метод Гоффман-Якобса является более быстрым, но менее чувствительным, чем комплексометрический метод.
Физиопатологические изменения. Нормальная сыворотка содержит 18–22 мг калия/100 мл, а цельная кровь – в среднем 170 мл) 100 мл. Следовательно эритроциты содержат почти 10-кратное количество калия по сравнению с сывороткой. Калий играет весьма важную роль в поддержании сердечного автоматизма за счет антагонизма калий-кальций и равновесия К/Са, весьма важного для сердечной функции. Кроме того, существует также антагонизм по отношению к натрию. Равновесие Na/K управляется кортиконадпочечниковыми гормонами. При болезни Аддиссона встречается нарушение равновесия в пользу калия, которое может быть восстановлено подвозом натриевых солей в избытке и максимальным снижением подвоза калиевых солей. И, наконец, калий принимает участие в глюцидном обмене при передаче фосфатной группы с аденозинтрифосфата на пировиноградную кислоту. Гиперкалиемии наблюдаются при заболеваниях, сопровождающихся более значительным разрушением эритроцитов, а также при диабете, циррозах печени, хронических артритах, некоторых легочных заболеваниях (плевритах и экссудативном туберкулезе) и изъязвлениях желудка и двенадцатиперстной кишки.
Кальций
Волюметрический метод
Принцип. Осаждение катиона Са ++ непосредственно из сыворотки без дезальбуминирования в виде оксалата кальция раствором оксалата аммония, согласно известного уравнения.
Реактивы.
- Оксалат аммония, насыщенный раствор.
- Серная кислота н/1.
- Перманганат калия 0,01 н. Приготовляют перед употреблением, разбавляя 1/10 раствор перманганата калия 0,1 н. Фактор (F) перманганата калия 0,01 н. определяют титрованием раствором щавелевой кислоты 0,01 н. В центрифужную Пробирку вводят 2 мл щавелевой кислоты 0,01 н. и 2 мл серной кислоты н. и титруют при температуре 60–70° перманганатом калия 0,01 н. до розового цвета, который должен быть устойчивым в течение 1–2 минуты.
Техника.
а) Осаждение кальция. В центрифужную пробирку из иенского стекла с коническим дном вводят 1 Мл негемолизированной сыворотки и добавляют 1 мл насыщенного раствора оксалата аммония. Оставляют в покое в строго вертикальном положении до следующего дня для осаждения кальция, затем центрифугируют 15 минут на больших оборотах (3 500–4 000 об/мин), для того, чтобы осадок отложился в верхушке конуса центрифужной пробирки. Надосадочную жидкость удаляют сифонированием или отсасыванием тонко вытянутой пипеткой Пастера, соединенной с водоструйным насосом. Для полного стечения жидкости пробирку держат 2–3 минуты отверстием вниз на фильтровальной бумаге. Затем осадок промывается 2–3 раза по 2 мл дистиллированной воды, хорошо взбалтывая. После каждого добавления промывочной воды тщательно центрифугируют, а воду удаляют сифонированием.
б) Титрование. Осадок растворяют в 2 мл серной кислоты н. (2), выдерживая пробирку в течение 1 минуты в кипящей водяной бане и помешивая стеклянной палочкой. В другой пробирке приготовляют слепой образец, используя для этого 1 мл дистиллированной воды и 1 мл серной кислоты н. Пробирки кладут в водяную баню и титруют при температуре 60–70° перманганатом калия 0,01 н. до бледно-розовой окраски, которая должна быть устойчивой в течение 1–2 минуты.
Комплексометрический метод
Принцип. Непосредственное титрование ионов кальция в сильно щелочной среде двухнатриевой солью этилендиаминтетрауксусной кислоты (ЭДТА) в присутствии мурексида в качестве индикатора.
Ионы кальция, вначале соединенные с индикатором (розовый цвет) затем реагируют количественно титрованием с помощью ЭДТА, выделяя индикатор, вследствие чего этот последний окрашивает раствор в фиолетовый цвет.
Реактивы.
- Раствор едкого натра 9 н. Растворяют 36 г вещества в дистиллированной воде, а после охлаждения объем доводят до 100 мл.
- Индикатор мурексид (пурпурат аммония). Используют тонко размельченную смесь мурексида и нитрата калия в соотношении 1/800.
- Раствор ЭДТА 0,01 н. В мерной колбе на 1000 мл растворяют 861 г сухого вещества в 200 мл дистиллированной воды, подщелачивая едким натром 10%, пока раствор не станет вполне прозрачным, затем дополняют до метки дистиллированной водой. 1 мл раствора ЭДТА 0,01 и. титрует 0,2 мг кальция. Для проверки можно приготовить эталон следующим образом: в фарфоровую чашку вводят 2 г карбоната кальция для анализа (точно отвешенного) и 1 мл соляной кислоты и выпаривают досуха. Осадок хлористого кальция растворяют в дистиллированной воде, переводят в мерную колбу на 1 000 мл, дополняют до метки. 1 мл содержит 0,8 мг кальция. Этот запасный раствор, разбавленный 1/10 содержит 0,08 мг кальция /мл, так что 5 мл (0,4 мг кальция) должны титроваться точно 1 мл ЭДТА 0,01 н.
Техника. Разбавляют 2 мл сыворотки в 48 мл дистиллированной воды, добавляют 0,4 мл едкого натра 9 и. и щепотку (несколько сантиграмм) индикатора (2). Титруют раствором ЭДТА 0,1 н. (3) до получения изменения окраски смеси от розового в фиолетовый цвет. Параллельно титруют слепой образец, используя вместо сыворотки дистиллированную воду. Значение полученное при титровании контрольного образца вычитается из значения (п).
Примечание. Метод довольно прост, отличается быстротой причем эти преимущества не влияют на точность результатов. Исключая осаждение, для которого необходимо 24 часа, он дает возможность произвести определение непосредственно после взятия материала.
Физиопатологические изменения. Сыворотка содержит 9–11 мг/100 мл, эритроциты 0,6–5,9 мг/100 мл, а цельная кровь 4-6 мг кальция/100 мл крови.
Сывороточный кальций состоит из двух фракций: ионизирующийся и неионизирующийся кальций, сочетающийся с сывороточными белками. Ионизирующийся кальций представляет собой физиологически активную фракцию и составляет 45–55% (4,75–6,25 мг/100 мл) общего кальция сыворотки.
В организме приблизительно 99% кальция находится в костной ткани, причем в первую очередь кальций играет пластическую роль. Кроме того, он имеет также динамическую роль в проницаемости мембран, водообмене, коагуляции крови. И наконец, кальций оказывает влияние на нейромышечный механизм, причем его снижение менее 3 мг/100 мл вызывает столбнячные явления. Регулирование обмена кальция подчиняется влиянию гормонов и витаминов D, А и С.
Гиперкальциемии встречаются при: гиперпаратиреоидизме, подагре, хроническом ревматизме, гипервитаминозе D (вызванном приемом чрезмерного количества витамина D),B некоторых случаях нефрита с уремией и др.
Гипокальциемии наблюдаются при гипопаратиреоидизме, недостаточности в витамине D, некоторых тяжелых формах нефрита и нефроза, а также при рахитизме, при котором снижается и содержание кальция в костях, в то время как содержание магния увеличивается. То же явление наблюдается и при других болезнях, сопровождаемые деминерализацией скелета.
Магний
Метод Веллуз
Принцип. После высушивания и прокаливания сыворотки, магний осаждают ортооксихинолином в виде нерастворимого оксихинолината магния. Этот последний бромируют избытком бромида и бромата калия.
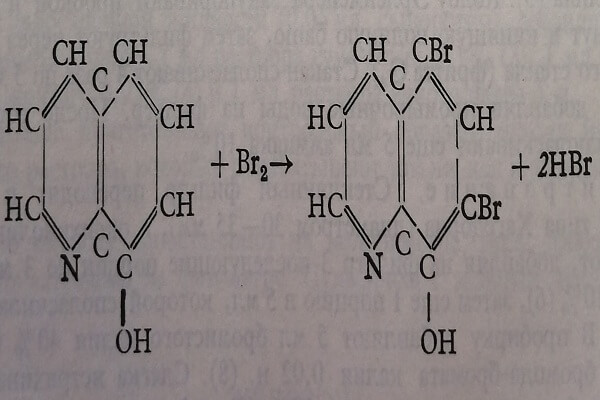
Избыток брома, обработанный йодистым калием выделяет йод, который титруют тиосульфатом натрия.
Реактивы.
- Соляная кислота 5%.
- Ледяная уксусная кислота 0,5%.
- Оксалат аммония 0,1 н.
- Аммиак 10%.
- Соляная кислота 10%.
- Бромистый калий 45%.
- Бромил-бромат калия 0,02 н. Приготовляют непосредственно перед употреблением, разбавляя раствор ОД н., получаемый следующим образом; точно отвешивают 50 г бромистого калия и 2,785 г бромата калия. Переводят в мерную колбу на 1000 мл, растворяют в дистилллированной воде и дополняют до метки.
- Йодистый калий 20%.
- Крахмал 1%.
- Тиосульфат натрия 0,02 н. Приготовляют непосредственно перед употреблением из тиосульфата 0,1 н.
Техника.
а) Высушивание и прокаливание сыворотки. В платиновую чашечку вводят 5 мл негемолизированной сыворотки, причем чашечку ставят в сушильный шкаф Хереуса при 105–110° в течение около 4–5 часов до получения сухого остатка. Этот последний осторожно прокаливают на газовой горелке, сначала при небольшом пламени, которое затем постепенно увеличивают, до получения белой золы. Оставляют для охлаждения, затем добавляют 2 мл соляной кислоты 5% (1) и выпаривают досуха на песочной бане в вытяжном шкафу или в сушильном шкафу. Осадок растворяют в 5 мл уксусной кислоты 0,5% (2) и переводят в колбу Эрленмейера на 50 мл с притертой пробкой, причем чашечку споласкивают 5 раз по 1 мл дистиллированной воды, добавляя промывочные воды в тот же сосуд.
б) Осаждение магния. Слегка встряхивают, добавляют 2 мл оксалата аммония 0,1 н. (3), 2 мл аммиака 10% (4) и 0,25 мл орто- оксихинолина (5). Колбу Эрленмейера закупоривают пробкой и помещают на 10 минут в кипящую водяную баню, затем фильтруют через пластинку из иенского стекла. Стакан споласкивают 4 раза по 5 мл аммиака 10% (4), добавляя промывочные воды на фильтр. После этого стенки фильтра споласкивают еще 5 мл аммиака 10%.
в) Титрование. Стеклянный фильтр переводят в широкую пробирку типа Хагедорна (диаметром 30–35 мм), а оксихинолинат магния растворяют, добавляя на фильтр 3 последующие порции по 3 мл соляной кислоты 10% (6), затем еще 1 порцию в 5 мл, которойсполаскивают стенки фильтра. В пробирку добавляют 5 мл бромистого калия 40% (7) и 5 мл раствора бромида-бромата калия 0,02 н. (8). Слегка встряхивают, затем добавляют 5 мл йодистого калия 20% (9) и 2 капли крахмала 1% (10). Выделяемый йод титруют тиосульфатом натрия 0,02 н. (11) до исчезновения синего цвета.
В другой пробирке Хагедорна приготовляют контрольный образец; для этого наливают 5 мл раствора бромида-бромата калия 0,02 н. и, добавляя 5 мл йодистого калия 20% и 2 капли крахмала 1%, титруют так же как и анализируемый образец.
Физиопатологические изменения. Нормальная сыворотка содержит 2,2–3 мг магния на 100 мл, а эритроциты – около 5 мг на 100 мл. В ряде явлений магний оказывает антагонистическое действие по отношению к кальцию. Кроме того, он играет важную роль активатора ряда энзимов, а также ингибитора для других энзимов. И наконец, магний участвует также в проницаемости клеточных мембран.
Авитаминоз D сопровождается 50% увеличением содержания магния в сыворотке.
Колориметрический метод
Принцип. Магний дает с титановым желтым красную окраску, интенсивность которой пропорциональна присутствующему в анализируемом образце количеству магния.
Реактивы:
- Раствор вольфрамата натрия 10%.
- Раствор серной кислоты 2/3 н.
- Раствор гума-гатли 1%.
- Раствор титанового желтого 0,05%.
- Раствор едкого натра 4 н.
- Стандартный раствор хлористого магния, содержащий 0,03 мг магния/мл.
Техника. В центрифужную пробирку наливают 1 мл сыворотки, 5 мл дистиллированной воды, 2 мл вольфрамата натрия 10% (1) и 2 мл раствора серной кислоты 2/3 н. (2). Встряхивают и фильтруют. К 5 мл прозрачной надосадочной жидкости (0,05 мл сыворотки) добавляют 1 мл дистиллированной воды, 1 мл раствора гума-гатли 0,1%, 1 мл раствора титанового желтого 0,05% (4) и 1 мл раствора едкого натра 4 н.
Параллельно приготовляют контрольный образец, исходя из 0,5 мл стандартного раствора, который обрабатывают так же как и анализируемый образец.
Красную окраску сопоставляют на колориметре типа Дюбоска или отсчитывают затухание на фотометре Пульфриха с зеленым фильтром на 530 мл.
Железо
Фотометрический метод
Принцип. Сывороточное железо, выделяемое соляной кислотой в виде двухвалентного иона и дезальбуминированное железо дает с о-фенантролином соединение красного цвета, исключительно устойчивое и пропорциональное количеству железа, вследствие чего его можно колориметрировать.
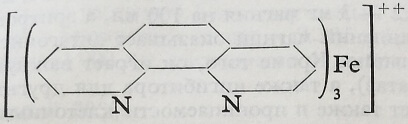
Реактивы.
- Соляная кислота н 6: разбавляют 1: 1 бидистиллированной водой соляную кислоту для анализа (удельный вес 1,19).
- Трихлоруксусная кислота для анализа 20%.
- нитрофенол 1% в спирте 95°.
- Аммиак для анализа 20%.
- Серная кислота 0,5 н.
- Гидрохинон 2%. Приготовляют непосредственно перед употреблением для каждой серии определений, растворяя 0,2 г чистого гидрохинона в 10 мл бидистиллированной воды, слегка нагревая и предварительно добавляя 1–2 капли концентрированной серной кислоты для анализа (7).
Техника.
а) Дезальбуминирование. В пробирку из иенского стекла наливают 2 мл негемолизированной сыворотки и 1 мл соляной кислоты 6 н. (1). Хорошо встряхивают и оставляют в покое на 10 минут. Затем добавляют 2 мл трихлоруксусной кислоты 20% (2). Снова встряхивают и оставляют в покое на 10 минут, затем фильтруют через небольшой количественный фильтр, свободного от железа.
б) Получение окраски. Из прозрачного фильтрата берут 2,5 мл (1 мл сыворотки) и переводят в градуированную пробирку на 10 мл, затем добавляют 1 каплю нитрофенола 1 % (3) и осторожно нейтрализуют аммиаком 20% (4), пока жидкость не приобретет бледно-желтую окраску, после чего по каплям добавляют серную кислоту 0,5 н. (5) до исчезновения желтой окраски. И наконец, добавляют 3 капли гидрохинона 2% (6) и 3 капли о-фенантролина 1% (7) и слегка встряхивают. Отсчет производится с особой точностью и отмечается объем жидкости, который составляет приблизительно 4 мл. Параллельно с этими операциями приготовляется контрольный образец, для чего вместо сыворотки берут 2 мл бидистиллированной воды. Контрольный образец обрабатывают так, как и анализируемый. При этом также отмечается объем Ук. Спустя 10 минут, отсчитывают затухание на фотометре Пульфриха с зеленым фильтром на 500 м(л и кюветой на 10 мм, используя в качестве компенсирующей жидкости бидистиллиро- ванную воду.
Примечания. Для фотометрического определения можно построить также калибровочную кривую, выражающую оптическую плотность (затухание), в зависимости от концентрации железа.




