Методы фотометрии в определении аналитов в биоматериалах
В данной статье рассмотрены физические свойства света, рефрактометрия, поляриметрия, методы фотометрических измерений, устройство фотометров и спектрофотометров, стандартизация фотометрических приборов.
Физические свойства света. Основные понятия
Многие определения в клинической лабораторной диагностике основаны на измерении лучистой энергии, испускаемой, поглощаемой, рассеиваемой и отражаемой в определенных условиях. Методы исследования веществ, основанные на их (веществ) способности порождать оптическое излучение или взаимодействовать с ним, называются оптическими.
Оптическое излучение представляет собой электромагнитные колебания определенного диапазона частот, распространяющихся в пространстве со скоростью света, которая в вакууме составляет 3 • 108 м/с.
Понятие «электромагнитное излучение» относится ко всем видам лучистой энергии: гамма- и рентгеновскому излучению, ультрафиолетовому, видимому и инфракрасному свету, а также к радиоволнам. Самая короткая длина волны и, соответственно, самые большие кванты – у гамма-лучей, испускаемых радиоактивными веществами; самые длинные волны, и, соответственно, самые малые кванты – у радиоволн.
Светом обычно называют ту область лучистой энергии, которая видна человеческим глазом, распространяя это понятие на близлежащие области ультрафиолетового и инфракрасного спектра света. Свет – одна из форм электромагнитного излучения, которое распространяется в виде волн и характеризуется частотой, т. е. числом колебаний в единицу времени (v), длиной волны (к) и постоянной скоростью распространения в вакууме с. Эти величины связаны между собой соотношением: v = с/Х.
Лабораторные специалисты обычно выражают длину волны света в метрических единицах – нанометрах: 1 нм = 1 ммк =10 А= = 10-9 м = 10-7 см. Человеческий глаз различает (видит) лучистую энергию в диапазоне примерно от 380 до 750 нм. При помощи приборов можно измерить свет и в более коротковолновой (ультрафиолетовой) и более длинноволновой (инфракрасной) области спектра.
Солнечный свет – это смесь различных длин волн, которую человеческий глаз воспринимает как белый. Различные цвета представляют собой компоненты солнечного света, соответствующие отдельным участкам его спектра (табл. 1.1).
Физические свойства света сложны. В одних случаях он ведет себя как электромагнитная волна, в других – это поток материальных частиц – фотонов. Энергия светового потока – энергия фотонов, или энергия излучения, прямо пропорциональна его частоте и обратно пропорциональна длине волны. Спектр излучения – функция распределения электромагнитной энергии в зависимости от частоты и длины волны. Излучение энергии на одной частоте и соответствующей ей длине волны называется монохроматическим излучением.
При взаимодействии света с веществом могут наблюдаться два случая:
- вещество достаточно прозрачно, поэтому свет, проходя через него, поглощается очень слабо. Отношение скорости света в вакууме к его скорости в данном веществе представляет показатель преломления этого вещества. Поскольку он во многом зависит от длины волны, свет при прохождении через прозрачную стеклянную призму разлагается в спектр по длинам волн. По обе стороны от видимого спектра располагаются невидимые лучи - ультрафиолетовые и инфракрасные;
- вещество поглощает значительную часть световой энергии. Энергия света согласно квантовой теории поглощается квантами. При этом отдельные молекулы, обладающие совокупностью близко расположенных один от другого энергетических уровней, могут, поглощая кванты света, переходить с относительно низкого энергетического уровня на более высокий. В таком «возбужденном» состоянии они способны флюоресцировать или подвергаться фотохимическим превращениям. В результате «возбуждения» они испускают электромагнитные волны разнообразных частот, образующих спектр испускания. При прохождении света через слой вещества оно поглощает те длины волн, которые само способно излучать в определенных условиях. Так образуется спектр поглощения. Таким образом, оптические методы количественного анализа веществ основаны на регистрации изменений, происходящих с лучом света при прохождении его через исследуемый раствор.
Классификация оптических методов количественного анализа в зависимости от принципа измерения представлена на схеме (рис. 1.1).
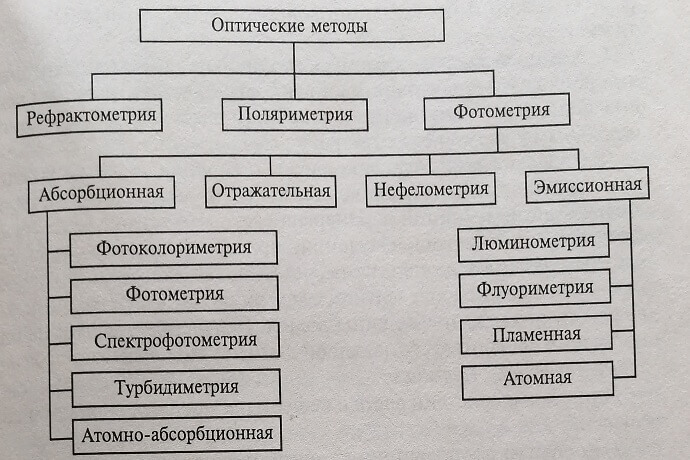
Рисунок 1.1. Классификация оптических методов исследований
Рефрактометрия
Это метод измерения показателя преломления света при прохождении его через оптически неоднородные среды. Ранее рефрактометрию применяли для определения содержания общего белка в плазме или сыворотке крови. Вследствие измерения при этом преломления света не только белками, но и небелковыми компонентами биожидкости рефрактометрический анализ дает ложнозавышенные результаты и не рекомендуется к применению в клинико-диагностических лабораториях.
Поляриметрия
Метод основан на свойстве прозрачных веществ вращать плоскость поляризованного луча света. В настоящее время этот метод применяют в миниатюризованном лазерном поляриметре МП 1010 (EKSMA; Латвия) для определения глюкозы в моче.
Принципы и виды фотометрии
Фотометрия – это измерение интенсивности света, прошедшего через раствор. Фотометрические методы – это методы количественного анализа, основанные на переведении аналитов в поглощающие свет соединения с последующим определением их количества путем измерения светопропускания или светопоглощения растворов. При фотометрии измерение энергии светового потока происходит с помощью фотоэлектрических приемников оптического излучения, или фотодетекторов, преобразующих световую энергию в электрический сигнал. С помощью этих приборов можно определять концентрацию аналитов по окраске растворов окрашенных веществ.
Колориметрия
Если при измерении не выделяется узкий диапазон длин волн, а измеряются характеристики всего светового потока, то такой метод называют колориметрическим. Метод представляет собой измерение интенсивности цвета раствора неизвестной концентрации путем сравнения его с интенсивностью цвета стандартного раствора. Предполагается, что толщину слоя одного из этих растворов изменяют, пока не будет достигнуто визуальное (видимое на глаз) равенство окрасок.
Спектрофотометрия
При выделении характерного для поглощения данным веществом оптического диапазона и проведении измерения на определенной длине волны речь идет о собственно фотометрическом методе. Фотометрию можно выполнять в разных вариантах: если есть возможность выделения только одного или нескольких спектральных интервалов с помощью светофильтров, то говорят о фильтровом фотометре, если существует монохроматор – устройство, позволяющее выделять пучок света с любой длиной волны, то говорят о спектрофотометрии.
Поток световой энергии, переносимый через единицу площади, называется интенсивностью потока световой энергии. Часть света, которая падает на оптическую среду (например, раствор исследуемого вещества) отражается, другая поглощается или рассеивается, а остальная проходит насквозь.
При измерении концентрации исследуемого вещества фотометрическим методом подбирают такие условия, при которых отраженным и рассеянным светом можно пренебречь. Поэтому количество прошедшего света равно количеству падающего за вычетом поглощенного. Отношение интенсивности потока световой энергии, прошедшего через слой исследуемого раствора I к интенсивности падающего (на кювету) потока световой энергии называется коэффициентом пропускания Т = I,/I0, или Т= 100%. Величина D= lgl/Т называется оптической плотностью. Величина оптической плотности безразмерна, но может исчисляться в беллах (Б). Для обозначения оптической плотности в инструкциях к реагентам и в зарубежной литературе по биохимическим исследованиям используют символ А. В отечественной литературе для обозначения оптической плотности стандартизован символ D.
Оптическая плотность – мера непрозрачности раствора — зависит только от толщины поглощающего слоя (l), или внутреннего размера кюветы (внутренняя длина кюветы, см); концентрации поглощающего вещества (С, г/л) и поглощающей способности исследуемого вещества в растворе (k): D = klC. Эта зависимость известна под названием закона Бугера-Ламберта-Бера. Коэффициент к — показатель поглощения, постоянная величина, зависящая от длины волны и природы вещества.
Если длину кюветы выражают в сантиметрах, концентрацию вещества в растворе в моль/л, то к называют молярным показателем поглощения. Молярный показатель поглощения является константой и характеризует свойство вещества поглощать свет на данной длине волны оптического излучения при определенных условиях: температуре, pH, растворителе и т.д. Его выражают в л/(моль-см)-1, а численное значение, таким образом, равно оптической плотности D раствора с концентрацией вещества 1 моль/л при длине кюветы 1 см. В системе СИ молярный показатель поглощения выражается в м2/моль, т. е. в величине оптической плотности, которой обладал бы раствор, на 1 м2 поверхности которого приходится 1 моль вещества. Численное значение ех в 10 раз меньше, чем при размерности л/(моль*см)-1.
Светопропускание имеет обратную и логарифмическую связь с концентрацией поглощающего вещества. Оптическая плотность, характеризующая поглощение, в соответствии с законом Бугера–Ламберта–Бера прямо пропорциональна концентрации растворенного вещества. При фиксированной длине кюветы / (в клинической химии принята стандартная кювета 1 см) оптическая плотность D и концентрация растворенного вещества С связаны через молярный показатель поглощения. Будучи специфичным для каждого вещества, он зависит от структуры вещества, характеризует собой способность молекул вещества поглощать свет с длиной волны X и не зависит от концентрации вещества. Показатель является функцией длины волны света, и поэтому зависимость е(Х) может служить количественной характеристикой спектра вещества.
Каждое вещество имеет свой спектр поглощения. Для разных форм вещества он разный, например для окисленных и восстановленных форм никотинамидаденинпиридиндинуклеотидов и их фосфатов.
Величину используют для характеристики веществ, оценки их чистоты и для сравнения чувствительности измерений различных производных веществ.
Часто линейная зависимость между концентрацией вещества и соответствующей ей величине оптической плотности в данных условиях, т.е. соответствие закону Бугера-Ламберта-Бера, имеет место лишь на определенном участке калибровочного графика, например в его начале, до определенной концентрации. В случае использования коэффициента поглощения к = D/ С, концентрация вещества для данного диапазона С - D/(kl). Так как к и l в данном случае постоянны, то их можно заменить параметром F, который называют фактором расчета. В этом случае формула упрощается: С = FD.
Для того чтобы вычислить величину F проводят калибровку — измеряют в соответствии с методикой оптические плотности (D) нескольких калибровочных растворов с известными концентрациями (С) и сопоставляют графически полученные значения D и С. Для этого строят градуировочный, или калибровочный график: на миллиметровой бумаге изображают систему координат, на которой по оси абсцисс (ось «х») откладывают значение концентраций вещества (С), по оси ординат (ось «7») – соответствующие им величины оптической плотности с поправкой на холостую пробу (AD). Если они пропорциональны друг другу, говорят, что калибровочный график – линейный и приведенной выше формулой можно пользоваться. Если пропорциональности нет, говорят, что зависимость – нелинейная и закон Бугера-Ламберта-Бера к данным условиям не применим.
Найти фактор расчета F можно несколькими способами.
В самом просто случае используют линейную часть калибровочного графика. Для этого на калибровочном графике в линейной части выбирают точку «n» и от нее проводят перпендикуляры к осям х и у. В точке пересечения перпендикуляра с осью х находят концентрацию определяемого вещества Сп, а с осью у – соответствующую этой концентрации величину оптической плотности ADn.
Закон Бугера-Ламберта-Бера лежит в основе всех методов колориметрии и фотометрии, независимо от того, в какой области спектра – видимой, ультрафиолетовой или инфракрасной – выполняют измерение, а также от того, каким способом измеряют интенсивность светового потока и как проводят расчет: по данным измерений на одной или нескольких длинах волн. Современные фотоэлектроколориметры, фотометры и спектрофотометры представляют собой настоящие анализаторы со встроенными микропроцессорами и компьютерами, имеющими программное обеспечение для проведения расчетов результатов и в тех случаях, когда калибровочный график не имеет линейного характера в соответствии с алгоритмами, характерными для поведения аналита и конкретного продукта реакции в данном методе.
Остановимся еще на некоторых видах фотометрии, используемых при выполнении различных исследований. Ранее всего были созданы фотометры и спектрофотометры, в которых луч света от источника излучения идет горизонтально — горизонтальная фотометрия.
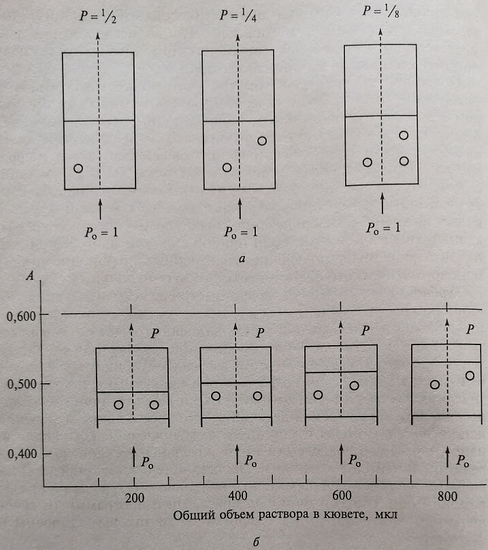
В 1968 г. финский врач О. Суованиеми разработал метод вертикальной фотометрии и основанный на нем полуавтоматический анализатор для биохимических исследований (FP 9, последующие варианты прибора – FP 900, FP 900М). При вертикальной фотометрии луч света идет снизу вверх или сверху вниз, а у измерительной кюветы только одна грань – нижняя, функцию верхней грани выполняет мениск жидкости. Было показано что поскольку общая масса абсорбирующего свет вещества в растворе всегда размещена между нулевым и верхним уровнями, то независимо от вертикального распределения молекул вещества и количества растворителя в кювете величина абсорбции света А равна специфической абсорбции исследуемого вещества (а), умноженной на его массу (т) и деленной на площадь поперечного сечения кюветы (51).
Поэтому случайное или предусмотренное методикой разбавление пробы не сказывается на результатах, так как уменьшение концентрации компенсируется увеличением столба жидкости (рис. 1.2). Выделенный интерференционным светофильтром монохроматический свет передается с помощью стекловолоконной оптики и проходит через коллимационные линзы (линзы, превращающие расходящиеся пучки света в параллельные) и через раствор в кювете. Реакцию выполняют в планшетах, состоящих в зависимости от конструкции и назначения прибора из 6, 8, 9 или 96 и более кювет, которые являются одновременно емкостями для проведения реакции и фотометрии. В одноканальных фотометрах для вертикальной фотометрии измерение оптической плотности происходит в каждой из кювет последовательно. В многоканальных фотометрах для иммуноферментных исследований (ридерах, считывателях) детекция прошедшего света происходит несколькими детекторами одновременно в нескольких кюветах.
Рис. 1.2. Схематическое представление зависимости результатов измерения в вертикальном фотометре от общего количества вещества, абсорбирующего свет (а), и отсутствие зависимости от длины пробега луча в исследуемом растворе и концентрации вещества в растворе (б)
Хотя в клинико-диагностических лабораториях достаточно широко используют простые спектрофотометры, в том числе для ручной работы, основная тенденция развития технической мысли идет в направлении создания специализированных лабораторных приборов для клинико-диагностических лабораторий и универсальных спектрофотометров для научных исследований, возможности которых по некоторым пунктам выходят за пределы потребностей клинической лаборатории.
Современный спектрофотометр – это полностью компьютеризированный полуавтоматический или автоматический прибор, который может проводить измерения с точным выделением требуемой длины волны монохроматического света в очень широком диапазоне длин волн – ультрафиолетовом, видимом и инфракрасном. Прибор основан на двухлучевой схеме. Компьютер обрабатывает результаты измерений, сохраняет их в электронной форме и выдает на дисплее. Для получения сопоставимых спектров для различных диапазонов длин волн прибор снабжен программой, которая обеспечивает получение равномерных по ширине пучков монохроматического света по всему рабочему диапазону.
Турбидиметрия
Это метод фотометрического измерения поглощения света взвешенными в растворе частицами определяемого вещества, т. е. измерение света, прошедшего через мутный раствор, подобно измерению абсорбции при фотометрии в направлении прохождения света. Поэтому в качестве турбидиметров можно использовать большинство фотометров для ручных и полуавтоматических измерений и биохимических автоанализаторов, основанных на фотометрической детекции. Чаще всего такие измерения используют в методах гомогенного иммунохимического анализа, например, при определении индивидуальных белков на основе реакции «антиген-антитело». Особенностью таких определений является нелинейный характер калибровочного графика и расчет результатов в соответствии с алгоритмами и программным обеспечением для нелинейных графиков, если таковые встроены в фотометр.
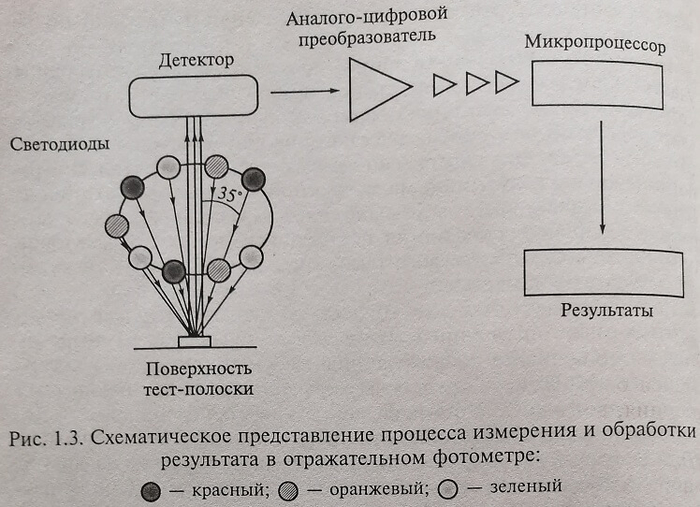
Отражательные фотометры, или рефлектометры
Это особый вид фотометрических устройств для количественного измерения света, отраженного поверхностью (рис. 1.3). В клинической лабораторной диагностике они находят применение в «сухой химии», когда цветную биохимическую реакцию проводят на полоске, в результате чего определенная ее зона окрашивается. В качестве источников света в таких системах использованы светодиоды, излучающие свет той длины волны, которая специально подобрана для определенной цветной реакции на исследуемой зоне диагностической полоски. Для детекции света, отраженного от окрашенных зон полоски, можно применять измерительные головки, воспринимающие свет спустя отрезок времени, соответствующий скорости развития окрашивания зоны, предназначенной для детекции определенного аналита. Особенность отражательной фотометрии заключается в том, что нужно измерить сумму световых потоков, которые отразились от исследуемой поверхности в разных направлениях.
Предварительно свет надо собрать в одно место. Для этого исследуемый объект помещают в сферу (шар), внутренние стенки которого равномерно отражают все цвета спектра. Лучи света, отраженные и рассеянные в разных направлениях, многократно отражаются от внутренней поверхности шара, внутри которого создается равномерная освещенность, интенсивность которой определяется суммой всего отраженного исследуемой поверхностью света. Сфера усредняет свет по всем направлениям. Фотоприемник вмонтирован в сферу и фиксирует освещенность внутри нее.
Методы фотометрических измерений
Как правило, для фотометрии выбирают ту область спектра, где поглощение максимально, обычно это увеличивает точность количественного измерения и повышает его чувствительность. Однако, с другой стороны, оптическая плотность не должна быть слишком большой, иначе количество прошедшего света мало, соответственно падает и становится ненадежным сигнал фотоприемника. Кроме того, длину волны выбирают так, чтобы по возможности уменьшить интерференцию (мешающее влияние) посторонних веществ. Так, щелочной пикрат при определении креатинина имеет пик в видимой области при длине волны 480 нм, но реактив сравнения (холостой опыт) сильно абсорбирует свет с длиной волны менее 500 нм, поэтому для измерения выбирают светофильтр 520 нм, что уменьшает влияние холостой пробы, улучшает точность и правильность результата.
Желательно, чтобы в выбранном для измерения спектральном участке кривая была по возможности горизонтальной, тогда некоторая немонохроматичность измерительного пучка мало сказывается на результатах. Если же она приходится на «склон» пика, то оказывается, что внутри данного пучка одни участки сильно поглощают свет, другие – мало, это приводит к тому, что закон Бугера-Ламберта-Бера не выполняется. Основной способ устранения мешающего влияния посторонних веществ и факторов (интерференции) — это вычитание оптической плотности холостой пробы из опытной.
Обычно холостую пробу готовят так же, как и исследуемую (опытную), с той разницей, что в нее не добавляют анализируемый материал, либо ставят реакцию таким образом, что в содержащей биоматериал и реактивы холостой пробе специфическая реакция, как в опытной пробе, не развивается.
Можно независимо измерить оптическую плотность опытной и холостой проб, а затем вычесть одну из другой либо установить начальную точку отсчета фотометра (100 % пропускание) по холостой пробе. Первый способ более трудоемок, но имеет преимущество в том, что необычное отклонение «фона», которое может быть признаком неправильного выполнения методики, сразу становится очевидным.
Интерференцию вследствие попадания загрязнений, небольшой мутности и царапин на стенках кюветы можно исключить или уменьшить, измеряя оптическую плотность на двух или трех длинах волн. По существу, это шаг в сторону хемометрии — высокотехнологического метода, который предполагает измерение на многих длинах волн и компьютерную обработку результатов, с тем чтобы вычленить небольшой полезный сигнал на фоне многочисленных помех.
В двухволновом методе измерения делают на максимуме пика (опорная, или основная, длина волны) и на уровне его основания (поддерживающая длина волны), полагая, что любые помехи в равной степени сказываются и на поглощении света, и на той и на другой длине волны, а исследуемое вещество специфически поглощает только на одной из них. Это так называемый бихроматический анализ, который широко применяется во многих приборах.
В трехволновом методе делают следующие измерения: одно до начала пика, а другое после него, затем на соединяющей их прямой находят то место, которое соответствует пику, и эту величину вычитают из значения для опытной пробы.
Различают измерения в конечной точке реакции, т.е. когда реакция уже завершилась, и изменение оптической плотности более не происходит в течение некоторого периода времени (реакция вышла на плато). Период выхода оптической плотности на плато и его продолжительность могут быть иногда довольно длительными, что имеет различное значение, в зависимости от того, каким образом выполняются измерения – ручным или автоматическим. При работе ручными методами выбирают такие методы, когда оптическая плотность в конечной точке реакции не изменяется в течение длительного времени (10, 30 мин и более), для того чтобы можно было точно выполнить достаточно большую серию измерений. Примерами могут служить определение общего белка по биуретовой реакции, когда при комнатной температуре образование биуретового комплекса происходит в течение 30 мин. Оптическая плотность при этом нарастает и через 30 мин выходит на плато, а далее стабильна по меньшей мере еще в течение 30 мин.
При определении мочевины уреазным методом с реакцией Бертло на аммиак оптическая плотность синего, или «изумрудного», комплекса стабильна в течение нескольких часов. Автоматизация таких методов требует сокращения времени реакции для получения рентабельной производительности анализаторов за счет изменения некоторых условий, например повышения температуры или использования другого принципа измерения — не в конечной точке реакции, а по «начальной скорости», т.е. наибольшей скорости реакции после ее запуска, поскольку в дальнейшем скорость реакции уменьшается. Этот метод используют как для определения активности ферментов, так и для установления концентрации некоторых субстратов, например в случае определения общего белка по биуретовой реакции на центрифужных анализаторах, которые позволяют проводить быстрые, с очень короткими интервалами времени (миллисекунды), и высокоточные фотометрические измерения.
Другой принцип фотометрического измерения основан на способе измерения оптической плотности в двух временных точках реакции: в начале и спустя 1-2 мин или более – принцип фиксированного времени. Условием использования этого способа измерения является сохранение линейной зависимости между концентрацией аналита и оптической плотностью комплекса, образующегося в ходе реакции. Если измерять оптическую плотность через короткие равные промежутки времени после добавления рабочего реактива к пробе (или пробы к рабочему реактиву) и перемешивания, начинается изменение оптической плотности, в котором можно выделить несколько периодов. Вначале, когда происходят неспецифические реакции, линейной зависимости изменения оптической плотности в равные интервалы времени не наблюдается. Это так называемая фаза «задержки» (lag phase delay), по окончании которой изменение оптической плотности носит линейный характер в зависимости от времени в течение некоторого периода, специфичного для данного метода, а затем по мере окончания реакции – вновь нелинейный. Измерения оптической плотности для расчета результата могут проводиться в двух точках линейной части этого графика. Такие методы проведения реакции и фотометрии называются еще двухточечными, или псевдокинетическими. Этот принцип известен в одноэтапных, простых, быстрых методах определения креатинина по реакции Яффе без осаждения белка, гексокиназном методе определения глюкозы, полностью ферментативном УФ-тесте определения мочевины, турбидиметрическом методе определения фибриногена, иногда в УФ-тестах определения активности аланиновой и аспарагиновой аминотрансфераз.
Принцип кинетического измерения, т.е.многократного (многоточечного) измерения оптической плотности после окончания фазы «задержки» через равные интервалы времени и расчета изменения ее в линейной части графика, отражающего зависимость изменения оптической плотности от времени после запуска реакции, широко применяют при определении каталитической активности ферментов или для ферментативного определения субстратов (глюкозы, креатинина, мочевины, мочевой кислоты и др.). Он получает все более широкое распространение в связи с внедрением в практику клинико-диагностических лабораторий полуавтоматических и автоматических анализаторов, основанных на фотометрии.
Осуществление таких измерений предъявляет особые требования к конструкции фотометров:
- выделение строго монохроматического светового потока, особенно для длин волн 340 и 405 нм за счет применения хороших интерференционных светофильтров в фотометрах или использования спектрофотометров;
- высокая точность измерения оптической плотности не только в диапазоне до 1,0 Б, но и в более высоком диапазоне – около 2,0 Б, что необходимо для реализации УФ-теста Варбурга;
- точное соблюдение температуры термостатирования не только при инкубации реактивов и развитии реакции, но и при фотометрическом измерении (общепринятым считается поддержание температуры в измерительной ячейке в пределах ±0,2 °С);
- оснащение компьютеризированных фотометров специальным программным обеспечением для расчета конечного результата на основе многократных измерений оптической плотности.
При фотометрической детекции результата в коагулологических методах используют принцип измерения фиксированной абсорбции: определяют время, в течение которого оптическая плотность продукта реакции, образующегося в растворе в кювете, достигает определенного значения, например 0,1 Б. Особенность технологии выполнения реакции и измерения светопоглощения в этих случаях заключается в том, что запуск реакции в кювете осуществляется с помощью специальных пипеток, соединенных с фотометром и встроенным в фотометр секундомером. Подобным образом определяют протромбиновое время, активированное частичное тромбопластиновое время (АЧТВ) в плазме методами с хромогенными субстратами.
Устройство фотометров и спектрофотометров
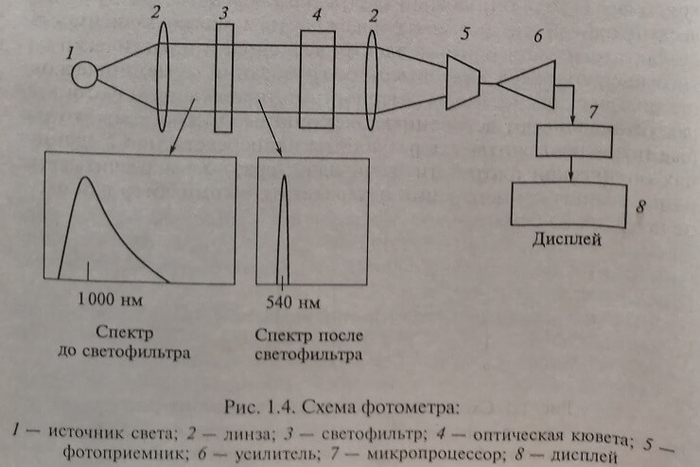
Оптические приборы, измеряющие полихроматический световой поток (в спектральной полосе 7-12 нм) только в видимом диапазоне света, называют фотоэлектроколориметрами. Приборы, измеряющие полихроматический световой поток в ультрафиолетовом, видимом и инфракрасном диапазонах называют фотометрами (рис. 1.4). Спектрофотометры — оптические приборы, разделяющие световой поток на непрерывный спектр и позволяющие измерять его на любой длине волны в пределах оптического диапазона. Фотометрия может выполняться по однолучевой или двухлучевой схеме.
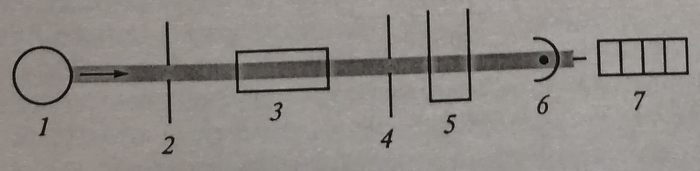
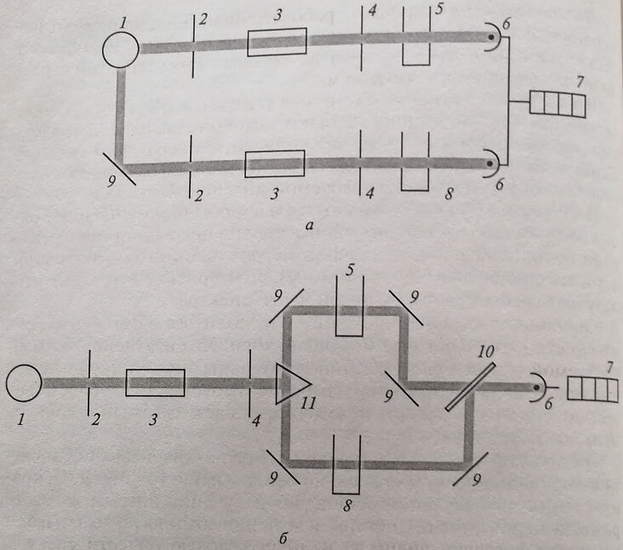
При однолучевом методе (рис. 1.5) с помощью фотоприемника (фотодетектора, сенсора) измеряют интенсивность светового потока в отсутствие кюветы с исследуемой пробой или когда она заменена кюветой с растворителем (холостой опыт), Затем ставят кювету с исследуемым раствором, снова измеряют количество прошедшего света и вычисляют величину оптической плотности по приведенной ранее формуле. В зависимости от конкретной конструкции прибора расчет выполняют с помощью встроенной микросхемы или по специальной шкале. Таким образом, фоновое (холостой опыт) и опытное измерения разнесены во времени, что может быть причиной ошибок, если источник света нестабилен.
Рис. 1.5. Схема однолучевого спектрофотометра
1 — источник света; 2 — входная щель; 3 — монохроматор; 4 — выходная щель; 5 — кювета; 6 — детектор; 7 — измерительное устройство
При двухлучевом методе (рис. 1.6) оба измерения выполняют одновременно. Это достигается за счет того, что источник света генерирует два луча одинаковой интенсивности: один из них проходит через опытную пробу (исследуемый раствор), другой через пробу сравнения (холостую), обычно один растворитель, затем их интенсивности сравнивают. Сравнение можно выполнять механически, в этом случае пучок света после пробы сравнения проходит через отверстие диафрагмы, сужая которое, добиваются равенства интенсивностей обоих пучков. Диафрагму приводят в движение барабаном, который обычно градуирован непосредственно в величинах оптической плотности.
Рис. 1.6. Схема двухлучевого спектрофотометра:
а – спектрофотометр с пространственным разделением лучей света: б – спектрофотометр с разделением лучей света во времени; 1 – источник света; 2 – входная щель; 3 – монохроматор; 4 – выходная щель; 5 – кювета с пробой; 6 – детектор; 7 – измерительный прибор; 8 – кювета с раствором сравнения (холостая проба); 9 – зеркало; 10 – прерыватель; 11– разделитель луча света
Равенство обоих пучков света можно оценить разными способами: визуально оценивая различие освещенности двух половин поля зрения, либо электрически, добиваясь равенства фототоков, о чем судят по положению стрелки гальванометра. Механический способ, несмотря на надежность и малую зависимость результатов от колебаний в электрической сети, практически не употребляют вследствие высоких требований к механической отладке, юстировке и равномерности потоков света. В фотометрах устанавливают встроенные электронные микросхемы, которые позволяют считывать результаты непосредственно в единицах оптической плотности, если надо, сразу же пересчитывать их в единицы концентрации и передавать в компьютер или распечатывать на бумаге.
Принципиальное различие между одно- и двухлучевой схемами остается, каждая из них имеет свои преимущества и недостатки. В двухлучевой схеме значение фона вычитается автоматически, в ней легче добиться стабильности результатов измерения на протяжении определенного периода времени (устранить дрейф нуля), но все ошибки и помехи, возникшие в канале сравнения (например, опалесценция раствора или появление в нем пузырьков) сказываются и на результатах опыта.
Любой фотометрический прибор – самый простой гемоглобинометр или совершенный спектрофотометр – имеет одинаковые элементы: источник света, устройство выделения нужной области спектра (монохроматическое устройство), кюветное отделение, фотоприемник (фотоэлектрический преобразователь), измерительно-регистрирующее устройство.
Источник света зависит от рабочего диапазона длин волн измерения. В качестве источников света в фотометрах используют несколько типов ламп, каждая из которых характеризуется различным сплошным излучением.
Вольфрамово-галогеновая лампа известна всем как используемый в домашних условиях источник света. Для продления жизни колбы в нее в малых количествах добавляют галоген. Серьезным недостатком этих ламп является их слабая способность возбуждать УФ-излучение требуемой интенсивности.
Дейтериевую дуговую лампу обычно располагают рядом с вольфрамово-галогеновой. Вместе они покрывают весь спектр длин волн, необходимый для фотометров видимого и ультрафиолетового диапазона (200-1100 нм). Дейтериевая дуговая лампа излучает слабый свет в видимой части спектра.
Основное преимущество ксеноновой лампы – это возможность получения с ее помощью хорошего излучения во всей требуемой области спектра. Дополнительных источников излучения при использовании этой лампы не требуется. Она более дорогая, содержит газ ксенон и возбуждает свет, сходный с солнечным светом.
Дуговые ртутные лампы (ртутно-кварцевые) относятся к смешанным (люминесцентно-тепловым) источникам. Основную часть их излучения составляет излучение плазмы дугового разряда паров ртути. Спектры излучения этих ламп охватывают ультрафиолетовую, видимую и инфракрасную области спектра. Сильное тепловое излучение, вызываемое лампами, нужно тем или иным способом отводить, чтобы не вызывать порчу светофильтров и не воздействовать на исследуемую пробу.
Широкое применение, особенно в приборах, созданных для решения конкретных аналитических задач (гемоглобинометры, нефелометры), находят светоизлучающие диоды – светодиоды – полупроводниковые устройства, излучающие монохроматический свет. Это – важное преимущество, поскольку отпадает необходимость в светофильтре, а кроме того, светодиод не нагревается во время работы.
Лазеры (аббревиатура от Light Amplification by Stimulated Emission of Radiation) – оптические квантовые генераторы – современные источники излучения, отличающиеся узким направленным пучком и когерентностью. Важнейшим свойством лазерного пучка является его монохроматичность и минимальное рассеивание в однородной среде. Полупроводниковые лазеры в отличие от других типов лазеров обладают рядом преимуществ: малыми размерами и компактностью; простотой конструкции; высокой эффективностью преобразования электрической энергии в энергию когерентного излучения; возможностью перестройки длины волны излучения и наличием большого числа полупроводников, непрерывно перекрывающих интервал длин.
Выделение области спектра
Поскольку для разных веществ воздуха характерно поглощение света на разных длинах волн, в приборах для фотометрии используют оптические средства (зеркала, линзы, светофильтры, монохроматоры) для выделения определенных интервалов и длин волн света. Нужные спектральные участки (полосы) выделяют с помощью светофильтров или монохроматоров. Наиболее простой и дешевый, поэтому наиболее распространенный, способ – использование светофильтров. С помощью монохроматора можно определить полный спектр, полученный от пробы. В фильтровых фотометрах монохроматор заменен светофильтрами.
Принцип действия светофильтров заключается в следующем. Свет от лампы концентрируется в узкий луч зеркалами и линзами перед тем, как направляется на фильтр. В приборах старой конструкции в качестве светофильтров использованы цветные стекла, в настоящее время их вытеснили интерференционные светофильтры, которые позволяют выделять полосы по 5-10 нм, в то время как для стеклянного фильтра полоса 50 нм – уже очень большое достижение. Характеристика фильтра – это ширина полосы пропускания в нанометрах, через которую проходит половина света.
Интерференционные светофильтры имеют удовлетворительную спектральную ширину полосы света и длину волны. С их помощью «паразитный» (побочный, а не с нужной длиной волны, свет) может быть исключен более эффективно, чем с помощью других фильтров. Интерференционные светофильтры состоят из двух полупрозрачных серебряных пленок и диэлектрического слоя между ними. Толщина диэлектрического слоя определяет длины волн света, который пропускает фильтр. Так же, как и решетка монохроматора подвергает дифракции более чем один спектр, интерференционные светофильтры пропускают свет с различными длинами волн, поэтому необходим дополнительный фильтр, который пресекает свет ненужных длин волн. Каждый фильтр пропускает довольно широкую полосу света, например 336-344 нм. Однако наивысшая интенсивность в середине этого диапазона – при 340 нм.
Кроме свойства обеспечения высокой монохроматизации света с относительно высоким его пропусканием интерференционные светофильтры обладают большой термоустойчивостью. Это связано с тем, что они не поглощают, а отражают прошедший сквозь них свет, что позволяет использовать светофильтры с высокоинтенсивными источниками светового (и теплового) излучения.
В настоящее время большинство фотометров и биохимических автоанализаторов оснащены интерференционными светофильтрами. Работая с ними, нельзя забывать два обстоятельства: во-первых, со временем они стареют, теряя свои оптические характеристики, во-вторых, они выделяют очень узкие пучки света, поэтому важно убедиться, что длина волны соответствует пику поглощения окрашенного продукта. Может случиться так, что два внешне одинаковых интерференционных светофильтра на самом деле пропускают свет с разными длинами волн.
Монохроматор действует следующим образом. Свет лампы с помощью линз и зеркал концентрируется в узкий световой пучок, направляемый на монохроматор, в котором он подвергается дисперсии, образуя спектр. Пройдя через монохроматор, полихроматический свет становится более или менее монохроматическим (в зависимости от щели на выходе устройства). Щель на выходе разделяет спектр таким образом, что выходящий свет имеет некоторый диапазон длин волн, например в пределах 539-541 нм.
Щель на входе представляет собой отверстие, через которое свет входит в монохроматор узким лучом во избежание избытка света на дифракционной решетке. Обычно щели на входе и выходе имеют одинаковую ширину.
Устройство дисперсии света
Узкий луч света фокусируется на дисперсионном устройстве – обычно дифракционной решетке. Последняя является сердцем монохроматора так же, как монохроматор является сердцем спектрофотометра. До использования решеток применяли призмы из стекла (для видимой области) или кварца (для ультрафиолетового излучателя). Они позволяют исследовать непрерывный спектр, особенность их заключается в большой неравномерности по длинам волн: в области коротких волн они позволяют выделять значительно более узкие пучки, чем в области длинных.
Дифракционная решетка представляет собой тщательно отполированную поверхность или зеркало, на которые нанесены параллельные штрихи (несколько сотен штрихов на 1 мм) или сделаны прорези на строго одинаковом расстоянии друг от друга, что обеспечивает дифракцию, поэтому под определенным углом отражается только свет соответствующей длины волны. При этом может быть более одной дифракционной серии, которые перекрывают друг друга. Они не будут интерферировать, если помещен дополнительный светофильтр, удаляющий побочные длины волн.
Преимущество дифракционной решетки по сравнению с призмой – более равномерное разрешение по длинам волн, линейная дисперсия на всем диапазоне видимого и ультрафиолетового спектра. От решетки спектр распространяется по направлению к щели на выходе и свет с единственной длиной волны проходит через нее и далее через кювету, достигая детектора. Обычно решетка вращается для контроля длины волны проходящего света.
Спектральная ширина полосы света равна ширине щели на выходе, если входная и выходная щели одинаковых размеров. Спектральную ширину не следует смешивать с естественной шириной полосы, которая представляет собой полуширину пика абсорбции (светопоглощения).
Спектральная ширина полосы света определяет разрешение спектрофотометра, т. е. его способность дифференцировать два очень близких друг к другу пика. Чем меньше ширина полосы, тем выше разрешение и тем более подробный спектр может быть получен. Щель на выходе оказывает наибольшее влияние на форму определяемого спектра: чем шире щель, тем шире пучок света и тем больше лучистой энергии попадает на приемник.
Сделав щель слишком широкой, можно выйти за пределы, в которых действует закон Бугера-Ламберта-Бера. Если щель слишком узкая, в приемник попадает мало лучистой энергии, что сказывается на точности измерения. В связи с тем что спектральное разрешение спектрофотметра зависит от длины волны, в разных спектральных участках оптимальны разные ширины щелей. В больших спектрофотометрах существуют встроенные программы, которые обеспечивают для каждой длины волны автоматический выбор рекомендованной ширины щели.
Кюветы и кюветные отделения
Кювета – это оптический компонент большинства фотометров и спектрофотометров. Луч света, прошедший через светофильтр или монохроматор, отражается зеркалом, проходит через кювету, содержащую реакционную смесь, и подвергается измерению. Кювета представляет собой емкость из прозрачного материала, которая устанавливается в кюветодержателе кюветного отделения. Обычно используют сменные, или, как их еще называют, сливные, кюветы квадратного сечения с длиной оптического пути 1 см, реже 0,5 или 0,3 см.
Кюветы имеют точную внутреннюю ширину (длина пути света), что обеспечивает возможность сравнения кювет по этому признаку. Различают три типа кювет, отличающихся качеством, при аттестованной длине пути света 10 мм: тип А – кюветы, имеющие длину пути, установленную с точностью до ±0,01 мм, тип В – до ±0,04 мм, и тип С – до ±0,3 мм. Различные кюветы обладают различными свойствами и светопропусканием, особенно в отношении УФ-света. Для измерений в УФ-свете обычно используют только кварцевые или кремниевые кюветы.
Разовые пластмассовые кюветы могут быть использованы не только для фотометрии, но и в качестве пробирок для выполнения подготовительных операций и анализа. В некоторых фотометрах используют кюветы, представляющие собой круглые пробирки для микроанализа, но, как правило, в таких приборах применяется измерение реакционной смеси на двух длинах волн (бихроматическое измерение) для исключения погрешностей, связанных со светорассеянием, вызванным непосредственно кюветой.
Широко распространены проточные кюветы, которые обычно снабжены устройством, позволяющим автоматически или полуавтоматически заполнять их до определенного уровня. Это облегчает и ускоряет работу, особенно, если фотометр соединен с печатающим устройством или напрямую связан с компьютером. Скорость заполнения проточной кюветы – несколько секунд. Объемы этих кювет исчисляются десятками микролитров (от 18 до 80 мкл) в зависимости от конструкции кюветы и прибора. Но для получения правильных результатов, как правило, требуется 300-500 мкл реакционной смеси, в том числе необходимых для промывания кюветы от предыдущей реакционной смеси и исключения влияния концентрации компонента в предыдущей пробе на последующую, т.е. ошибки от так называемого «переноса».
Некоторые современные фотометры имеют одновременно две встроенные кюветы, что позволяет не тратить время на смену кюветодержателей для различных кювет. Большинство современных фотометров и спектрофотометров имеют термостатированные кюветные отделения или блоки для поддержания постоянной температуры до 37 °С, которую контролируют специальные устройства. Это позволяет проводить измерения при фиксированной температуре, что особенно важно для кинетического определения активности ферментов.
Для исключения различий между кюветами, особенно при работе на спектрофотометрах, для измерения в кюветодержатель кроме кюветы, содержащей опытную пробу, помещают кювету с жидкостью для сравнения (холостая проба). Свет одного и того же луча направляется через обе кюветы полупроницаемым зеркалом или через отражающий прерыватель света. Это важно для анализа, при котором нулевая (базовая) линия измеряется одновременно.
Детектор
В конце своего пути луч света достигает детектора, который преобразует поток света (фотонов) в поток электронов (электрический ток). Существует несколько типов устройств для этих целей, имеющих разную способность в выполнении этого преобразования – это фотоэлементы, фотосопротивления, фотодиоды и фотоумножители.
Принцип действия фотоэлементов основан на явлении фотоэффекта, которое заключается в том, что при действии света вещество (как правило, одновалентный металл – цезий и др.) испускает электроны, которые в безвоздушном пространстве лампы устремляются от фотокатода к аноду. На практике выделяют два типа фотоэлементов – с внутренним и внешним фотоэффектом. Фотоэлементы с внешним фотоэффектом могут быть вакуумными и газонаполненными. Вакуумные фотоэлементы обладают меньшей фото чувствительностью, чем газонаполненные.
Освобождение электронов происходит и в полупроводниках, что увеличивает их электропроводность при освещении. Самым большим преимуществом фотодиодов является их малый размер. Они могут быть расположены в ряд, образуя диодный массив. Когда диодный массив расположен прямо за решеткой поперек спектра, требуется меньше оптических компонентов. Кювета должна быть расположена перед монохроматором, и это является недостатком для нестабильных веществ. Диоды могут регистрировать интенсивность поступающего света, так что весь спектр может быть определен с помощью массива диодов.
В настоящее время лучшие фотодиоды разработаны для улучшения детекции УФ-света. Детекция ими в области длин волн от 250 до 1000 нм используется уже на практике. Фотоумножители обнаруживают длины волн в широких пределах. Когда фотон входит в детектор, он ударяется о металлическую поверхность и освобождает один или более электронов из этой поверхности. Электроны ударяются о вторую металлическую поверхность, При этом освобождается еще большее количество электронов. После приблизительно десяти таких этапов электронный поток измеряют для расчета количества фотонов, которые вошли в детектор.
В качестве фотоприемников для видимой и ультрафиолетовой областей используют в основном вакуумные фотоэлементы, реже фотоумножители, для инфракрасной области – фотосопротивления. На приборах прежней конструкции используется компенсационная схема измерения – оптическая либо электрическая. При оптической схеме, вращая барабан, связанный с диафрагмой, добиваются равенства световых потоков. При электрической схеме, вращая ручки потенциометра, добиваются электрической компенсации фототока. И в первом, и во втором вариантах о наступлении момента компенсации судят по показаниям индикатора на панели прибора. Отсчет делают по положению барабана или ручек потенциометра. В выпускаемых в настоящее время приборах практически всегда световой поток вызывает пропорциональный его интенсивности фототок, который измеряется цифровым вольтметром, вся дальнейшая обработка информации выполняется в цифровой форме.
Измерительно-регистрирующие устройства
Такие устройства подразделяют на показывающие, регистрирующие и печатающие, аналоговые и цифровые. В показывающих приборах наблюдаемая величина определяется по шкале механического или электрического отсчетного устройства. Регистрирующие приборы выполняют автоматическую графическую регистрацию результата.
Аналого-цифровые преобразователи, встроенные в большинство современных фотометров, наряду с печатающими устройствами (принтерами) позволяют получать результат в распечатанном виде непосредственно в единицах концентрации или активности аналита.
Стандартизация фотометрических приборов
Правильность фотометрических измерений оценивают по результатам исследования стандартных образцов (эталонов), свойства которых считаются известными. Поскольку фотометрическое измерение дает два вида результатов, одни из которых выражены в единицах длин волн (частоты), а другие – оптической плотности (пропускания), в фотометрии используют стандарты для поверки шкалы длин волн и шкалы оптической плотности, или пропускания. Как средства измерения, к которым фотометры, спектрофотометры и анализаторы на их основе, используемые в лабораториях медицинских организаций, относятся в соответствии с законодательством Российской Федерации, они подлежат обязательной сертификаций и периодической (не реже 1 раза в год) поверке в эксплуатации.
Стандартизацию можно выполнять по эталонным светофильтрам с редкоземельными элементами, обладающими весьма узкими полосами поглощения. Для приборов с узкой шириной полосы пропускания используют хлорное оксидное олово, имеющее очень узкие полосы пропускания: 279,3; 278,6; 333,8; 360,8; 418,5; 536,4; 637,5 нм, для широкополосных приборов – дидимиевый фильтр, имеющий максимум пропускания при 530 нм (зеленая область). Стеклянные фильтры умеренного нейтрального стекла в сертификатах позволяют проверять калибровку фотометров на четырех длинах волн от 440 до 635 нм. Стеклянные оптические меры для поверки фотометрических приборов непосредственно являются средствами измерения, они занесены в Государственный реестр средств измерения и могут быть использованы для этого и в повседневной практике.
В связи с тем, что поверочными средствами практические работники клинико-диагностических лабораторий часто не располагают, некоторые характеристики фотометров (правильность, линейность показаний, их вариация) могут быть проверены также с помощью специально приготовленных растворов – жидких индикаторов. Эти растворы в определенной области спектра имеют постоянные спектральные характеристики. Характеристики некоторых растворов приведены в табл. 1.2. Методика приготовления растворов приведена далее.
1. Бихромат калия высушить при температуре 100-110 °С в течение двух часов, охладить в эксикаторе при комнатной температуре. Растворить 200 мг вещества в 3 000 мл дистиллированной воды, добавить 0,34 мл концентрированной 70 % хлорной кислоты. Количественно перенести в мерную колбу на 4000 мл. Довести объем до метки дистиллированной водой. Перемешать. Хранить раствор плотно закрытым в темной посуде. Кроме того, для проверки точности измерения оптической плотности используют и другой раствор бихромата калия. Для его приготовления реактив высушивают при температуре 110 °С в течение 1 ч, навеску 0,0500 г растворяют в 1 л серной кислоты концентрацией 0,005 моль/л. Оптическая плотность на длине волны 350 нм в кювете 10 мм при температуре 15-25 °С против серной кислоты концентрацией 0,005 моль/л должна составлять 0,536±0,005. Природная ширина полосы растворов бихромата при длине волны 350 нм – 63 нм; для спектрофотометров с шириной щели менее 6 нм этот раствор должен выявлять пик абсорбции при 350 нм.
2. Сульфат никеля высушить в эксикаторе при комнатной температуре в течение 48 ч. В мерной колбе на 1 000 мл растворить 30,4523 г NiS04 • 6Н20 в 800 мл дистиллированной воды, добавить 9 мл концентрированной 70 % хлорной кислоты. Довести объем до метки дистиллированной водой. Перемешать. Хранить раствор плотно закрытым в темной посуде.
3. Сульфат кобальта аммония высушить в эксикаторе при комнатной температуре в течение 48 ч. В мерной колбе на 1 000 мл растворить 39,5250 г вещества в 800 мл дистиллированной воды. Добавить 9 мл концентрированной 70 % хлорной кислоты. Довести объем до метки дистиллированной водой. Перемешать. Хранить раствор плотно закрытым в темной посуде.
4. Сульфат кобальта аммония в количестве 14,481 г растворить в 10 мл концентрированной серной кислоты. Количественно перенести в мерную колбу на 1 000 мл, содержащую 400 мл дистиллированной воды. После достижения раствором комнатной температуры довести объем до метки дистиллированной водой. Перемешать. Хранить раствор плотно закрытым в темной посуде.
5. Сульфат меди в количестве 20 г растворить в 10 мл концентрированной серной кислоты, количественно перенести в мерную колбу на 1 000 мл и довести объем при комнатной температуре до метки дистиллированной водой. Хранить раствор плотно закрытым в темной посуде.
6. Хромат калия в количестве 40 мг растворить в 600 мл раствора едкого кали концентрацией 0,05 моль/л в мерной колбе на 1 000 мл, затем довести объем до метки раствором едкого кали концентрацией 0,05 моль/л.
Растворы 1, 2, 3 приготавливают путем разведения основного раствора жидкого индикатора: 1 – основной раствор жидкого индикатора; 2 – основной раствор жидкого индикатора в двукратном разведении; 3 – в четырехкратном разведении; растворы 1-5 разводят дистиллированной водой; раствор 6 – раствором едкого калия концентрацией 0,05 моль/л.
Области применения фотометрии в клинической лаборатории и аналитике
Современная фотометрическая лабораторная техник представлена приборами различной степени сложности, что позволяет выбрать тот вариант фотометра, который наиболее соответствует конкретным условиям и задачам данной лаборатории. Наиболее распространены фотометры и фотоэлектроколориметры, которые обеспечивают потребности основной массы клинико-диагностических лабораторий при выполнении большей части биохимических (более 80 %), коагулологических, иммунохимических исследований как в ручном, так и в полуавтоматическом режиме.
Фотометры для ручных методов и программируемые полуавтоматические фотометры небольшой производительности применяют в основном как базовые приборы в клинико-диагностических лабораториях небольшой мощности и экспресс-лабораториях. Полуавтоматические фотометры с встроенными термостатами для инкубации реакционной смеси и термостатируемыми проточными кюветами для микроанализа можно использовать не только как базовые приборы в небольших или средних по мощности лабораториях, но и как вспомогательные приборы к автоматическим анализаторам.
Фотометры, оснащенные встроенными микропроцессорами, управляющими процессами фотометрического измерения, термостатирования, расчета и автоматической выдачи результатов, контролирующими этапы работы прибора, могут быть одноканальными (для последовательного измерения реакционных смесей в одной кювете) или многоканальными (для одновременного измерения их в нескольких кюветах). Такие приборы называют полуавтоматическими фотометрическими анализаторами. Их производительность подчас сравнима с автоанализаторами, хотя работа на них всегда требует участия оператора в процессе анализа. Некоторые из них при дооснащении дилютором и самплером могут быть преобразованы в так называемые серийные (batch) автоанализаторы.
Широкое применение находят также многоканальные фотометры, в которых применена оптическая схема, позволяющая установить одновременно большое количество (до 96) проб и фотометрировать их либо одновременно, либо последовательно за короткий промежуток времени. Такие приборы работают по однолучевой схеме. Многоканальный фотометр – это шаг к биохимическому анализатору, от которого он отличается тем, что автоматизирует только фотометрию, т.е. один из многих этапов анализа. В многоканальных фотометрах использована вертикальная схема измерения.