Туляремия
Туляремия – инфекционная болезнь, протекающая у людей обычно с затяжной лихорадкой, явлениями токсико-аллергического или септического характера и с вовлечением в процесс лимфатической системы. Это типичный зооантропоноз с природной очаговостью.
Этиология
Возбудителем туляремии является мелкая грамотрицательная бактерия Francisella tularensis. Внутри этого вида различают 3 географические расы (голарктическая, среднеазиатская, неарктическая), отличающиеся некоторыми биологическими особенностями (М. А. Айкимбаев, 1966; Н. Г. Олсуфьев, 1970). В окрашенных мазках возбудитель имеет кокковидную или палочковидную форму (диаметр 0,3-0,5 мк), но могут встречаться и более мелкие клетки (0,15 мк и меньше). Электронномикроскопическое изучение бактерий туляремии выявило существование гладкоконтурной оболочки, клеточной стенки, представленной трехслойной мембраной и внутренним слоем, цитоплазматической мембраны, гранулярной цитоплазмы, нуклеоида, а также наличие вокруг клеток капсулоподобного слизистого вещества (И. Б. Павлова и соавт., 1967). Микроб туляремии – факультативный анаэроб (Н. Г. Олсуфьев, 1975). Оптимальная температура для его выращивания на плотной питательной среде 36-37° при рН-7,0.
Возбудитель устойчив к воздействию внешней среды. Лиофильное высушивание в условиях вакуума с последующим хранением культур при низких температурах обеспечивает сохранение жизнеспособных туляремийных микробов многие годы.
В вирулентной форме туляремийные бактерии содержат оболочечный VI и соматический О антигенные комплексы (Н. Г. Олсуфьев и О. С. Емельянова, 1957). При этом вирулентные и иммуногенные свойства возбудителя связаны с Vi-антигеном. В ответ на заражение в организме человека (или животного) вырабатываются антитела, выявляемые реакциями агглютинации, преципитации, связывания комплемента. Большое практическое значение имеет явление аллергизации организма в результате заражения F. tularensis.
Распространенность
Природные очаги, связанные преимущественно с дикими грызунами, межзональны; они известны во многих странах Европы, Северной Америки, в некоторых странах Азии и Южной Америки. В СССР туляремия обнаружена во всех союзных республиках кроме Киргизии.
Клинические черты
Люди любого возраста и пола восприимчивы к туляремийной инфекции. Заболевание начинается остро подъемом температуры до 38-39° после инкубационного периода (чаще 3-7 дней). На фоне явлений интоксикации организма (головная и мышечные боли, слабость, иногда рвота и т. д.) возникает воспаление лимфатических узлов, расположенных вблизи места проникновения возбудителя. В зависимости от механизма заражения и локализации первичных поражений различают бубонную, язвенно-бубонную, глазо-бубонную, ангинозно-бубонную, абдоминальную и легочную клинические формы болезни (Г. П. Руднев, 1960 и др.). Наиболее часто возникают язвенно-бубонная, ангинозно-бубонная и легочная формы болезни.
Прогноз при туляремии благоприятный. Клинический диагноз без лабораторного подтверждения и данных эпидемиологического анализа затруднен. В плане дифференциальной диагностики следует исключать бруцеллез, дифтерию, брюшной тиф, риккетсиозы, грипп, туберкулез, эпидемический паротит, чуму, лимфадениты иной природы и др.
Эпидемиология
Эпидемиологические особенности туляремии определяются многими причинами, из которых наиболее существенны следующие:
а) Способность возбудителя болезни адаптироваться к различным видам животных, что обусловливает множественность потенциальных источников инфекции. В СССР установлена естественная зараженность более 80 видов позвоночных животных. Однако эпидемиологическая роль их далеко не одинакова; она зависит от быстроты размножения представителей данного вида, с чем связана возможная плотность популяции, а также от степени восприимчивости (чувствительности) животного к возбудителю туляремии.
В СССР образование и сохранение природных очагов туляремии обеспечивают только некоторые массовые виды млекопитающих, наиболее чувствительных к этой инфекции (I группа по Н. Г. Олсуфьеву). Сюда относятся водяные крысы, обыкновенные полевки, домовые мыши и другие животные. Туляремия у этих зверьков протекает, как правило, в виде острого септического процесса, вызывающего их гибель и сопровождающегося накоплением в их органах и тканях огромного количества возбудителя, что и обусловливает эпизоотологическое значение этих грызунов. Передача заразного начала в их популяциях происходит через воду и корм, загрязненные выделениями больных животных, а также посредством вшей, клещей, блох.
б) Многообразие переносчиков, относящихся к различным классам членистоногих. В распространении туляремии среди людей особое значение имеют некоторые двукрылые: комары (Culex, Anopheles, Aedes), слепни (златоглазки, дождевки) и др. В организме этих насекомых, заражающихся при кровососании больных или павших животных, а также через водоемы, бактерии туляремии могут переживать в течение нескольких дней. Формирование и поддержание природных очагов туляремийной инфекции в значительной мере связано с зараженностью иксодовых клещей родов Dermacentor, Ixodes, Rhipicephalus, Haemaphysalis и Hyalomma, в которых бактерии туляремии сохраняются длительно, но без трансовариальной передачи потомству.
Кроме иксодовых клещей в распространении туляремии среди животных могут принимать участие гамазовые клещи, многие виды блох и другие кровососущие членистоногие. Кроме того доказана возможность сохранения возбудителя туляремии в естественных условиях в организме некоторых гидробионтов (пиявки, моллюски и другие) в случае обитания их в инфицированных водоемах.
в) Стойкость возбудителя туляремии, способность его к длительному переживанию вне организма, определяет значение различных факторов передачи инфекции (воды, зерна, фуража, пищевых продуктов). В открытых водоемах, например, бактерии туляремии при низких температурах могут сохраняться в течение нескольких месяцев, с чем связано неоднократное выделение культур из одного водоисточника на протяжении различных сезонов года. Высокая устойчивость возбудителя туляремии к пониженной температуре позволяет допустить, что грызуны, павшие осенью или зимой, могут оказаться источником весенней эпизоотии следующего года.
г) Высокая инфекциозность бактерий туляремии для человека в сочетании с устойчивостью обусловливает множественность путей передачи возбудителя и возможность заболевания в результате проникновения его через кожу и слизистые глаза, через рот и верхние дыхательные пути. С этим связано многообразие клинических проявлений болезни, равно как существование различных типов вспышек туляремии, характеризующихся эпидемиологическими особенностями. В последнее время в СССР заражение с наибольшей частотой обусловливается трансмиссивным путем, а также при употреблении инфицированной воды Реже заболевания связаны с обмолотом зерновых.
В пределах нашей страны выделяют следующие ландшафтные типы природных очагов туляремии: степной, луго-полевой, пойменно-болотный, предгорно-ручьевой, лесной и тугайный. Каждый из них отличается своеобразием структурной организации и характером эпидемиологической проявляемости. Большая доля заболеваний людей связана с очагами пойменно-болотного и луго-полевого типов.
Противоэпидемические и профилактические мероприятия должны быть основаны на результатах широкой эпидемиологической и эпизоотологической разведки. Данные ее определяют размеры специфической вакцинации и контингенты, подлежащие прививкам, равно как комплекс истребительных мероприятий в отношении грызунов и кровососущих членистоногих.
Лабораторная диагностика
Своеобразие туляремийной инфекции определяет практическое значение лабораторных методов исследования как для диагностики, так и для решения вопросов эпидемиологического характера.
Обнаружение зараженных животных и клещей
Заболевания грызунов всегда предшествуют возникновению эпидемических вспышек. Размеры последних зависят прежде всего от интенсивности эпизоотии и от ряда других факторов биотического, абиотического и социально-экономического характера. Выяснение эпизоотологического состояния местности в отношении туляремии составляет основу для прогнозирования этой инфекции и для своевременного проведения профилактических мероприятий.
Применение лабораторных приемов должно сочетаться с санитарно-эпизоотологической разведкой обследуемой территории путем осмотра местности или объекта, сбора и анализа материалов о численности и видовом составе грызунов и насекомоядных, опроса населения для выяснения заболеваний среди зверьков и гибели их. Уточняются также места наибольшего их скопления.
Основные места сбора трупов и отлова грызунов определяются плотностью популяции на отдельных участках, обнаружением падежа среди мелких млекопитающих и степенью потенциальной эпидемиологической опасности определенных объектов. Должны привлекать особое внимание элеваторы, мельницы, бойни, склады пищевых продуктов как животного, так и растительного происхождения, в том числе холодильники, равно как пекарни, кухни. Обследуют также амбары, погреба, конюшни, коровники, свинарники. Местами гнездования полевых грызунов обычно являются запасы сена, корнеплодов, скирды необмолоченного зерна, ометы соломы, причем зверьки обнаруживаются в самом нижнем слое растительного сырья.
Наиболее типичными патолого-анатомическими изменениями при туляремии у грызунов являются инъецированность сосудов кожи, увеличение лимфатических узлов, увеличение печени и селезенки, наличие в этих органах мелких сероватого цвета некротических узелков, воспалительные изменения легких, геморрагии в них.
Зараженность животных устанавливают при помощи следующих методик: прямой бактериоскопии, использования иммуно-люминесцентного метода, посева в питательные среды, а также путем биологических проб и применения других иммунологических способов.
Бактериоскопический метод (микроскопирование фиксированных и окрашенных по Романовскому-Гимзе мазков-отпечатков из органов животных) надо рассматривать как ориентировочный. Бесспорно положительные результаты можно получать лишь при высокой концентрации возбудителя в органах грызунов. Это имеет место на высоте эпизоотии, особенно при исследовании павших животных. В этих случаях в мазках обнаруживаются большие скопления кокко-бактерий сиреневатого цвета.
Для оценки количества микроорганизмов в мазках-отпечатках пользуются следующей условной четырехбалльной шкалой Д. А. Голова и Н. Г. Олсуфьева.
- 1 балл – одиночные микробы или небольшие их скопления не в каждом поле зрения;
- 2 балла – та же картина, но в каждом поле зрения;
- 3 балла – большое количество скоплений в каждом поле зрения;
- 4 балла – сплошные колонии или большое число крупных скоплений в каждом поле зрения.
Иммунолюминесцентный метод предпочитают применять в виде прямой реакции, обладающей высокой чувствительностью. Этот способ сочетает в себе демонстративность прямой микроскопии и иммунологическую специфичность. Обычно специфические сыворотки конъюгируют с изотиоцианатом флуоресцеина; при наслаивании меченой сыворотки на мазки-отпечатки из органов животных, найденных павшими, а также на гистологические срезы или кишечники иксодовых клещей, при положительной реакции возникает яркое зелено-желтое свечение бактерий. Для дифференцирования специфической люминесценции от неспецифического свечения элементов ткани прибегают к контрастирующей окраске препаратов смесью специфической сыворотки и бычьего альбумина, меченного родамином. Этот прием создает окраску оранжево-красного цвета посторонних частиц, на фоне которого отчетливо выявляется зелено-желтое свечение бактерий туляремии.
Иммунолюминесцентный способ подкупает своей простотой и обеспечивает возможность проведения массовых исследований; тем не менее, он является сигнальным и должен быть подтвержден, также как и положительный результат прямой микроскопии, выделением культуры возбудителя.
Бактериологическое исследование трупов грызунов (без признаков гниения), а также зверьков, пойманных живыми (в случае обнаружения при вскрытии характерных для туляремии патолого-анатомических изменений), производят путем посева органов и тканей на специальную желточную среду Мак-Коя. Ее готовят следующим образом. Свежие куриные яйца моют щеткой с мылом в теплой воде, обтирают спиртом и обжигают на пламени. Извлеченные желтки собирают в стерильный сосуд, куда добавляют стерильный физиологический раствор в соотношении 60 частей желтка и 40 физиологического раствора. Смесь разливают по 5л в стерильные пробирки и свертывают в скошенном положении в течение часа в аппарате Коха при 75° с дополнительным получасовым нагревом до 80°. Стерильность среды контролируют выдерживанием на протяжении суток в термостате при 37°. Для обеспечения наибольшей репродукции возбудителя необходима свежесть среды и известная степень ее влажности, достигаемая наличием конденсационной воды на дне пробирок. Посев производят путем втирания кусочка исследуемого органа в поверхность скошенной желточной среды, начиная с нижней ее части, или отпечатками срезанного органа на поверхности среды. Для лучшего распределения посевного материала пробирки оставляют на 30 минут в горизонтальном положении, после чего ставят в штативах в термостат при 37°.
Рост бактерий туляремии обнаруживается в зависимости от концентрации их в исходном материале через двое-трое суток и позже. Принято выдерживать посевы в термостате до 10 дней.
Посев материала может быть произведен и на агаровую кровяную среду О. С. Емельяновой. Она состоит из гидролизата рыбной муки 20 мл, гидролизата желатины 10 мл, аутолизата дрожжей 2,5 мл, хлористого натрия 0,5 г, цистина 0,1 г, агара 1-2 г, дистиллированной воды 100 мл. pH среды 7,2-7,4. После стерилизации в среду, охлажденную до 45°, добавляют 10 мл свежей кроличьей или лошадиной дефибринированной крови» после чего ее разливают в пробирки и скашивают или разливают в чашки Петри. Правильно приготовленная среда Емельяновой должна быть красного цвета. Ее применяют для посева взвеси из растертых органов животного. Она обладает высокой чувствительностью и позволяет обнаруживать и единичные колонии бактерий туляремии.
Идентификацию выросших культур осуществляют путем микроскопирования окрашенных мазков из колоний, окрашивания мазков специфической флуоресцирующей сывороткой, испытания вирулентности на лабораторных животных и в опытах агглютинации противотуляремийной сывороткой.
Результаты выборочного бактериологического исследования грызунов, а также учет их численности и видового состава составляют основу суждения об эпизоотологическом состоянии местности в отношении туляремии.
Для выделения культур от мелких млекопитающих, наряду с посевом, используют метод биологических проб на белых мышах или (реже) на морских свинках.
Кусочки органов измельчают в физиологическом растворе и полученную взвесь вводят под, кожу подопытным животным. Органы загнивших трупов зверьков втирают в депилированые участки кожи; в этих же случаях материалом для исследования может служить мозг трубчатых костей грызунов; взвесь мозга в физиологическом растворе вводят подопытным животным под кожу.
При наличии в материале бактерий туляремии белые мыши реагируют на заражение остро протекающим септическим процессом и погибают в течение нескольких дней. Культуру возбудителя выделяют от них путем посева органов на упомянутые специальные питательные среды.
Малая концентрация возбудителя может не вызвать гибели лабораторных животных. В этих случаях необходимо прибегнуть к пассированию заразного начала путем введения новым лабораторным животным взвеси растертой в физиологическом растворе селезенки основного подопытного животного, забитого через 15 дней после заражения.
При массовых обследованиях грызунов и других мелких млекопитающих нередко прибегают к постановке групповых биологических проб. В этом случае подопытных животных заражают смесью органов от группы зверьков одного вида (до 10 экземпляров), отловленных в одних и тех же или близко расположенных местах обитания.
При оценке результатов посевов и биологических проб надо иметь в виду возможность возникновения среди грызунов эпизоотий туляремии в сочетании с другими инфекциями, например, стрептококковой или листереллезной.
При эпизоотологическом обследовании с целью выявления природных очагов туляремии лабораторному изучению подвергают мелких млекопитающих, отловленных живыми или трупы икеодовых клещей, а при определенных эпидемиологических показаниях –кровососущих двукрылых и воду из открытых водоемов и колодцев. При невозможности бактериологического исследования на месте органы вскрытых животных помещают в консервант, например, в смесь одной части парафина и 10 частей вазелинового масла, простерилизованный в течение 45 минут в водяной бане.
Серологическое подтверждение туляремии у животных осуществляют обычно при помощи реакции агглютинации (РА) и реакции преципитации (РП). С этой целью возможно также применение реакции пассивной гемагглютинации (РПГА) и нейтрализации антител.
РА применяют при исследовании домашних и более крупных диких животных, т. е. тех видов, у которых инфекция протекает доброкачественно. В качестве антигена используют туляремийный диагностикум, который добавляют в каждую пробирку с различными разведениями испытуемой сыворотки по 0,5 мл (исходная концентрация антигена 1 миллиард микробных клеток в 1 мл). Сыворотки разводят начиная с 1:5. Пробирки помещают в термостат на 2 часа. Учет результатов производят на следующий день Реакцию считают положительной при условии полного или почти полного склеивания микробной взвеси. Титры РА у животных, перенесших туляремию, сохраняются в течение двух-трех месяцев; они обычно невысоки, порядка 1:10-1:80.
При исследовании мелких мышевидных грызунов может быть применена РП. Для этой цели кусочек селезенки, взятой при вскрытии, растирают в ступке с 3-5 мл физиологического раствора; взвесь органа прогревают в водяной бане в течение 15 минут при температуре кипения воды и фильтруют через асбестовую вату до получения прозрачного экстракта. Последний в объеме 0,2-0,3 мл осторожно наслаивают по стенке пробирки на такой же объем агглютинирующей туляремийной сыворотки. В положительных случаях на месте соприкосновения сыворотки и фильтрата образуется кольцо помутнения беловатого цвета.
РПГА ставят с антигенным или с антительным эритроцитарным диагностикумами. С антигенным диагностикумом она может быть применена для исследования сывороток сельскохозяйственных и диких животных, равно как с диагностическими целями у людей. С антительным эритроцитарным диагностикумом постановка реакции целесообразна для подтверждения инфицированности (наличия антигена) трупов животных. РПГА чувствительнее РА, однако ее применение в практике ограничено из-за отсутствия коммерческого выпуска упомянутых диагностикумов.
Методика постановки РПГА при туляремии (с антигенным эритроцитарным диагностикумом) описана И. С. Мещеряковой (1964) в следующем виде: антиген (полученный по Буавену) разводят фосфатно-буферным раствором при pH 6,4. Из осадка отмытых 2-3 раза физиологическим раствором бараньих эритроцитов готовят (на физрастворе) 2,5% суспензию. Эритроциты сенсибилизируют в течение 3 часов при 37° антигеном из расчета 1 мг антигена на 1 мл взвеси эритроцитов. Затем эритроциты промывают 2—3 раза раствором, содержащим 0,4% нормальной кроличьей сыворотки, и тем же раствором доводят до исходной (2,5%) концентрации.
Исследуемые сыворотки инактивируют 30 мин при 58°. Для удаления гетерогенных антител к 2 объемам исследуемой сыворотки добавляют 1 объем осадка отмытых нормальных бараньих эритроцитов. Смесь выдерживают 10 мин при комнатной температуре и центрифугируют 5 мин при 3000 об/мин. Затем сыворотку отделяют от осадка и используют в РПГА. Исследуемые сыворотки разводят физиологическим раствором, содержащим 1% нормальной кроличьей сыворотки, ранее прогретой при 56° и истощенной описанным выше способом. К каждому разведению сыворотки добавляют по 1-2 капли сенсибилизированных эритроцитов. Реакцию учитывают через 2 часа при комнатной температуре и на следующее утро после выдержки в холодильнике. Реакция сопровождается контролями: исследуемой сыворотки и несенсибилизированных эритроцитов, растворителя сыворотки и несенсибилизированных эритроцитов, растворителя сыворотки и сенсибилизированных эритроцитов. Титр сыворотки учитывают по её последнему разведению, где агглютинат покрывает все дно пробирки.
У подопытных животных гемагглютинины появляются уже на первой неделе и достигают наивысшего титра на 14-21 сутки.
Титры РПГА значительно выше титров РА и достигают у животных 1:4000 при свежем инфицировании. При ретроспективной диагностике они невысоки как у животных, так и у людей (диагностический титр 1:160 и выше).
Кроме РПГА антигенные и антительные эритроцитарные диагностикумы могут быть использованы в реакции нейтрализации антител, подробно изученной И. С. Мещеряковой. Они изложены в новой сводке Н. Г. Олсуфьева (1975).
В зависимости от степени чувствительности зверьков к бактериям туляремии концентрация их в организме оказывается далеко не одинаковой, что приходится учитывать при выборе способов лабораторного обследования.
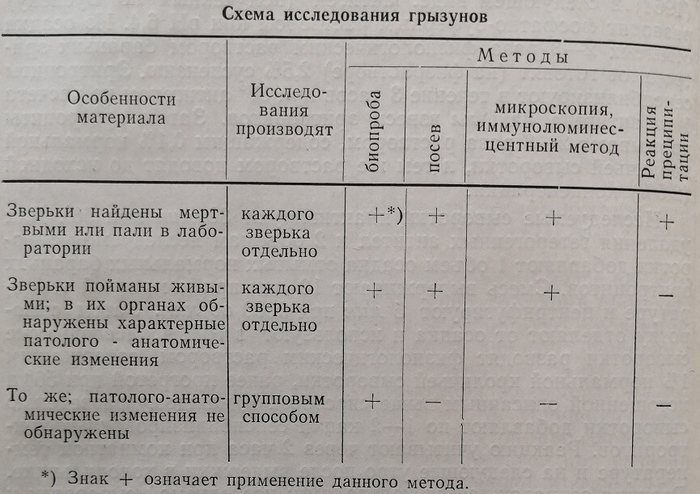
В результате сравнительной оценки перечисленных методик с учетом особенностей исследуемого материала может быть предложена следующая схема (табл.).
Применение перечисленных способов позволяет не только выявить эпизоотию туляремии, но дает возможность определять границы очага инфекции в природе, выяснить степень активности его, а также ориентироваться в вопросе об основном резервуаре инфекции в данных конкретных условиях.Эпизоотическое состояние местности в отношении туляремии непременно должно быть учтено при решении вопроса о допустимости акклиматизации в ней промысловых животных, чувствительных к возбудителю туляремии, например, ондатры.
Определение зараженности членистоногих, животных-гидробионтов и объектов внешней среды
Для определения зараженности членистоногих, а также воды, зерна, пищевых продуктов и других возможных факторов передачи возбудителя туляремии прибегают обычно к методу биологических проб.
Членистоногих, собранных непосредственно в природе или снятых с животных, группируют по видовому признаку и месту сбора. Половозрелых иксодовых клещей дважды промывают 70° спиртом, встряхивая их в пробирке, несколько раз промывают в стерильной воде, после чего измельчают. Личинок и нимф
иксодовых клещей многократно промывают стерильным физиологическим раствором и растирают в ступке до получения гомогенной взвеси. Ее вводят подкожно морским свинкам (3,0-5,0 мл) или белым мышам (0,5 мл). В этом объеме может содержаться до 50 взрослых иксодовых клещей или нимф, до 100 личинок, 75-100 блох или иных мелких членистоногих (вшей, гамазовых клещей). При изучении слепней им предварительно отстригают конечности и крылья; комаров растирают целиком. Материал для одной биопробы может включать до 50 слепней и до 100 комаров.
Частота положительных результатов исследования членистоногих значительно варьирует в зависимости от эпизоотической обстановки и тем самым может служить ее показателем.
При исследовании воды подопытных животных заражают также подкожно (белым мышам вводят до 1 мл, морским свинкам до 10 мл). Для концентрации возбудителя в пробах воды прибегают к предварительному отстаиванию или центрифугированию ее, а также к методам коагуляции или фильтрации через мембранные фильтры с последующим (перед заражением животных) подращиванием бактерий в течение одного-двух дней в жидкой желточной среде Дрожевкиной (10% куриного желтка и 90% физиологического раствора, смешанные в стерильных условиях).
При исследовании гидробионтов (ручейников, бокоплавов и др.), их промывают в нескольких порциях стерильной воды, соединяют в группы по 5-10 экземпляров и растирают в физиологическом растворе. Полученную взвесь вводят подопытным животным.
При анализе зерна или фуража с взятых проб (5-10 г) делают смыв в двойном по весу количестве физиологического раствора и этот материал вводят подкожно белой мыши (0,5 мл) или морской свинке (4-5 мл).
Выявление заболеваний, в том числе протекающих нетипично или бессимптомно
Выявление всех заболеваний, в том числе и наиболее легкими и тем самым трудно диагностируемыми формами туляремийной инфекции, имеет существенное значение, так как позволяет судить об истинных размерах вспышки и косвенно о массивности эпизоотии, способствует установлению источников и путей передачи возбудителя и определению иммунной прослойки населения.
А. Биологические пробы
В зависимости от клинической формы заболевания материалом для заражения животных являются: кровь (на первой неделе лихорадки), соскоб со дна язвы в месте входных ворот инфекции (первая неделя), отделяемое слизистой глаза (в течение двух недель при глазо-бубонной форме), пунктат бубона (на протяжении двух недель со времени его возникновения; пунктируют периферическую, не размягченную еще часть лимфатического узла), слизь из зева (при наличии ангины).
В зависимости от загрязненности исследуемого материала посторонней микрофлорой его вводят подопытным животным подкожно, внутрибрюшинно или путем втирания в депилированные участки кожи.
Б. Иммунологические методы
1. Реакция агглютинации – один из наиболее часто применяемых способов лабораторной диагностики заболеваний туляремией. Для постановки ее используют диагностикум из убитых бактерий туляремии, выпускаемый институтами вакцин и сывороток.
Минимальным диагностическим титром считают положительную реакцию в разведении сыворотки 1 : 100 при условии полного склеивания микробной взвеси и обязательного нарастания титра реакции в течение заболевания.
Агглютинины в убедительных титрах обнаруживаются в крови больных людей относительно поздно: частота положительных реакций на первой неделе не превышает 10%, на второй неделе положительные ответы могут быть получены примерно в 60%, а далее – в 80-95%. После перенесенной инфекции специфические антитела сохраняются в сыворотке в невысоких титрах порядка 1 :50–1 :100 на протяжении ряда месяцев, что позволяет при этих сроках ретроспективно устанавливать природу болезни. При однократной постановке реакции обнаружение «следовых» антител может оказаться причиной диагностических ошибок.
Вследствие антигенной общности бруцелл и бактерий туляремии могут возникать перекрестные реакции с этими антигенами, но с гомологичным антигеном титры оказываются более высокими.
Кроме обычной постановки РА в пробирках применяют также ускоренный способ в виде так называемой кровяно-капельной пробы (на стекле). Для нее предложен специальный антиген, представляющий концентрированную взвесь убитых бактерий туляремии в дистиллированной воде. Эта проба очень удобна при работе в полевых условиях: постановка ее не требует пункции вены, отстаивания сыворотки и термостата. К капле крови, полученной уколом мякоти пальца и помещенной на предметное стекло, добавляют каплю антигена. После перемешивания стеклянной палочкой обоих ингредиентов, при наличии в испытуемой крови специфических антител, появляется зернистая агглютинация, особенно ясно выступающая при покачивании стекла. Возникновение ее в течение первой минуты расценивают как положительную реакцию в титре не менее чем 1 :100.
При множественных заболеваниях, туляремийная природа которых уже установлена, когда основной задачей массового серологического обследования является обнаружение всех инфицированных, следует предпочесть кровяно-капельную пробу как наиболее простую и обеспечивающую быстрое получение ориентирующего ответа. При наличии же одиночных заболеваний, этиология которых еще не определена, необходимо применять «пробирочный» способ, так как он позволяет судить о нарастании титра специфических антител и, следовательно, обеспечивает суждение о специфичности реакции. В целях серологического подтверждения заболеваний как и для постановки ретроспективного диагноза с успехом может быть применена РПГА.
2. Аллергический метод. Больные и перенесшие туляремию люди отвечают местной аллергической реакцией на внутрикожное или накожное введение им антигена, приготовленного из бактерий туляремии. Положительная реакция возникает обычно начиная с 4-5 дня заболевания, т. е. раньше обнаружения специфических антител, и поэтому диагностическое значение ее Выше, чем серологических проб.
Перенесшие туляремию сохраняют способность положительно реагировать на введение им туляремийного антигена – «тулярина».
Этот препарат вводят внутрикожно в объеме 0,1 мл в ладонную поверхность предплечья или накожно, путем нанесения насечек через каплю тулярина, в средней трети плеча. При обоих способах у сенсибилизированных людей спустя 24-48 часов появляется краснота и инфильтрат в месте введения тулярина. Величина этих изменений на коже характеризует силу реакции.
Определение контингентов, подлежащих прививкам против туляремии, и учет эффективности вакцинации
Плановая широкая вакцинация против туляремии организуется по эпидемиологическим показаниям.
Проводившаяся в первые послевоенные годы систематическая иммунизация населения отечественной живой вакциной Гайского и Эльберта создала во многих местностях значительную иммунную прослойку в отношении этой инфекции. С другой стороны, эпидемиологическая (эпизоотологическая) разведка территорий, осуществленная органами здравоохранения и научно-исследовательскими учреждениями, уточнила ареалы природных очагов туляремии и позволила в связи с этим сузить показания к прививкам в ряде административных подразделений страны.В настоящее время сохранена практика обязательной вакцинации определенных групп населения, подвергающихся повышенному риску заражения в связи с выполняемой ими работой сюда относятся охотники за водяной крысой, ондатроловы, лица занятые заготовкой, приемом и хранением шкурок этих зверьков, а также члены их семей. Вакцинацию этих категорий производят перед началом заготовительного сезона.
Плановыми прививками охватывают также работников совхозов, зерно- и овощехранилищ, элеваторов, мельниц, предприятий по переработке сельскохозяйственных продуктов, животноводческих и птицеводческих ферм, лиц, проживающих в поймах рек, если эти местности неблагополучны по туляремии.
Кроме отвода от прививок по обычным медицинским противопоказаниям для парэнтерального введения бактерийных препаратов, от прививок освобождаются болевшие туляремией и ранее привитые при наличии у них положительной реакции на тулярин. Предварительный отбор болевших туляремией по показаниям кожной аллергической пробы необходим, так как перенесшие эту болезнь могут остро реагировать на прививку повышением температуры и увеличением регионарных лимфатических узлов, что может приводить к кратковременной утрате трудоспособности.
Путем применения кожной аллергической пробы получают представление о величине иммунной прослойки среди населения или отдельного коллектива как в результате перенесения болезни, так и вследствие активной иммунизации. Не существует, к сожалению, способов, позволяющих дифференцировать причины сенсибилизации организма. Состояние иммунности после прививок, также как и в результате перенесения болезни обусловлено размножением в организме возбудителя, а также разрушением бактерий туляремии под влиянием защитных механизмов. Процесс искусственной иммунизации, как и естественного инфицирования сопровождается возникновением повышенной чувствительности к повторному введению данного антигена,, что и учитывают при помощи кожной аллергической пробы.
Ревакцинацию производят также по эпидемиологическим показаниям не ранее, чем через 5 лет после вакцинации, причем лишь в тех случаях, когда выборочное обследование привитых показывает, что менее 75% из них положительно реагируют на тулярин.
Проверку успешного развития вакцинального процесса проводят через 12-15 дней после прививки путем втирания капли вакцины в насечки кожи на плече оспопрививательным пером.